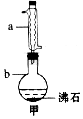
 乙酸乙酯是制藥工業和有機合成中的重要原料,實驗室制備乙酸乙酯的實驗裝置(夾持及加熱裝置已略去)、有關數據和實驗步驟如表所示:
乙酸乙酯是制藥工業和有機合成中的重要原料,實驗室制備乙酸乙酯的實驗裝置(夾持及加熱裝置已略去)、有關數據和實驗步驟如表所示:
| 物質 | 相對分子質量 | 密度/(g?cm-3) | 沸點/℃ | 在水中的溶解性 |
| 乙醇 | 46 | 0.789 | 80 | 以任意比互溶 |
| 乙酸 | 60 | 1.045 | 118 | 易溶 |
| 乙酸乙酯 | 88 | 0.902 | 77 | 難溶 |
①向儀器b中加入9.5mL乙醇(過量)和6mL乙酸,再緩慢加入2.5mL濃硫酸,混合均勻后,加入沸石,然后裝上冷凝管(如圖甲所示)。
②小火加熱儀器b,緩慢回流0.5h,待瓶內反應物冷卻后,將回流裝置改成蒸餾裝置,加熱蒸出乙酸乙酯。
③向餾出液中緩慢加入5mL飽和碳酸鈉溶液,振蕩,直至不再有二氧化碳氣體產生,然后將混合液轉移至分液漏斗中,分去水層,將有機層依次用5mL飽和食鹽水和5mL飽和氯化鈣溶液洗滌后,轉移至錐形瓶中,加入少量無水硫酸鎂固體,靜置片刻,過濾除去硫酸鎂固體,然后將有機層進行蒸餾純化,收集76~78℃時的餾分,得到4.2g乙酸乙酯。
請回答下列問題:
(1)實驗原理:乙酸與乙醇在催化劑存在的條件下加熱可以發生酯化反應生成乙酸乙酯,請用氧同位素示蹤法寫出CH3CO18OH與CH3CH2OH發生酯化反應的化學方程式
CH3CO18OH+CH3CH2OHCH3COOCH2CH3+H218O
濃硫酸
△
CH3CO18OH+CH3CH2OHCH3COOCH2CH3+H218O
。濃硫酸
△
(2)儀器a的名稱為
球形冷凝管
球形冷凝管
,儀器b的規格為 B
B
(填字母)。A.25mL
B.50mL
C.250mL
D.500mL
(3)步驟③中,將餾出液經飽和碳酸鈉溶液處理后的混合液置于分液漏斗中,振蕩后靜置,水層在
下層
下層
(填“上層”或“下層”)。(4)在步驟③中,加入少量無水硫酸鎂固體的作用是
干燥除水
干燥除水
。(5)酯層厚度的標定:加熱回流一段時間后再蒸出產物,為了更好地測定有機層厚度,可預先向飽和碳酸鈉溶液中加入1滴試液,現象是
碳酸鈉溶液層呈紅色,上層呈無色
碳酸鈉溶液層呈紅色,上層呈無色
。(6)該實驗中乙酸乙酯的產率為
45.7%
45.7%
(計算結果精確到0.1%)。【考點】乙酸乙酯的制取.
【答案】CH3CO18OH+CH3CH2OHCH3COOCH2CH3+H218O;球形冷凝管;B;下層;干燥除水;碳酸鈉溶液層呈紅色,上層呈無色;45.7%
濃硫酸
△
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/5/23 20:38:36組卷:18引用:1難度:0.5
相似題
-
1.下面是甲、乙、丙三位同學制取乙酸乙酯的過程,請你參與并協助他們完成相關實驗任務.
【實驗目的】制取乙酸乙酯
【實驗原理】甲、乙、丙三位同學均采取乙醇、乙酸與濃硫酸混合共熱的方法制取乙酸乙酯.
【裝置設計】甲、乙、丙三位同學分別設計了下列三套實驗裝置:
請從甲、乙兩位同學設計的裝置中選擇一種作為實驗室制取乙酸乙酯的裝置,較合理的是(選填“甲”或“乙”).丙同學將甲裝置進行了改進,將其中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是.
【實驗步驟】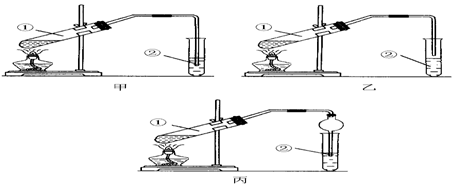
(1)按丙同學選擇的裝置組裝儀器,在試管中先加入3mL乙醇,并在搖動下緩緩加入2mL濃硫酸充分搖勻;冷卻后再加入2mL冰醋酸;
(2)將試管固定在鐵架臺上;
(3)在試管②中加入適量的飽和Na2CO3溶液;
(4)用酒精燈對試管①加熱;
(5)當觀察到試管②中有明顯現象時停止實驗.
【問題討論】
a.步驟(1)安裝好實驗裝置,加入樣品前還應檢查;
b.寫出試管①發生反應的化學方程式(注明反應條件);
c.試管②中飽和Na2CO3溶液的作用是;
d.從試管②中分離出乙酸乙酯的實驗操作是.發布:2024/12/30 19:30:2組卷:43引用:7難度:0.5 -
2.在酯化反應實驗中制得的乙酸乙酯中混有少量的乙酸,應選用下列哪種試劑洗滌除去( )
A.乙醇 B.飽和碳酸鈉溶液 C.水 D.NaOH溶液 發布:2024/12/30 8:30:1組卷:39引用:3難度:0.9 -
3.乙酸乙酯是重要的有機合成中間體,廣泛應用于化學工業。實驗室利用如圖A裝置制備乙酸乙酯。
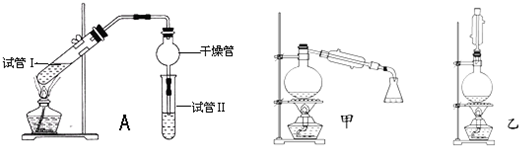
(1)若實驗中用乙酸和含18O的乙醇作用,該反應的化學方程式是:。與教材采用的實驗裝置不同,此裝置中采用了球形干燥管,其作用是。
(2)為了證明濃硫酸在該反應中起到了催化劑和吸水劑的作用,某同學利用上圖所示裝置進行了以下4個實驗。實驗開始先用酒精燈微熱3min,再加熱使之微微沸騰3min。實驗結束后充分振蕩小試管Ⅱ再測有機層的厚度,實驗記錄如下:
①實驗D的目的是與實驗C相對照,證明H+對酯化反應具有催化作用。實驗D中應加入鹽酸的體積和濃度分別是實驗編號 試管Ⅰ中試劑 試管Ⅱ中試劑 有機層的厚度/cm A 2mL乙醇、1mL乙酸、
1mL 18mol?L-1濃硫酸飽和Na2CO3溶液 3.0 B 2mL乙醇、1mL乙酸 0.1 C 2mL乙醇、1mL乙酸、
3mL 2mol?L-1H2SO40.6 D 2mL乙醇、1mL乙酸、鹽酸 0.6 mL和mol?L-1。
②分析實驗(填實驗編號)的數據,可以推測出濃H2SO4的吸水性提高了乙酸乙酯的產率。
(3)若現有乙酸90g,乙醇138g發生酯化反應得到88g乙酸乙酯,試計算該反應的產率為。
(4)現擬分離含乙酸、乙醇和水的乙酸乙酯粗產品,如圖是分離操作步驟流程圖。圖中內為適當的試劑,內為適當的分離方法。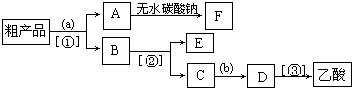
①試劑a是;分離方法②是,分離方法③是。分離方法①是分液,在具體操作中應充分振蕩,然后靜置,待分層后(填標號)。
A.直接將乙酸乙酯從分液漏斗上口倒出
B.直接將乙酸乙酯從分液漏斗下口放出
C.先將水層從分液漏斗的下口放出,再將乙酸乙酯從下口放出
D.先將水層從分液漏斗的下口放出,再將乙酸乙酯從上口放出
②在得到的A中加入無水碳酸鈉粉末,振蕩,目的是。
(5)為充分利用反應物,甲、乙兩位同學分別設計了如圖甲、乙兩個裝置(乙同學待反應完畢冷卻后,再用飽和碳酸鈉溶液提取燒瓶中的產物)。你認為最合理的是。發布:2024/12/30 19:0:1組卷:84引用:3難度:0.1


