九年級同學在實驗室進行氧氣的制備和性質實驗:
①A組同學用氯酸鉀、二氧化錳和如圖裝置進行實驗。
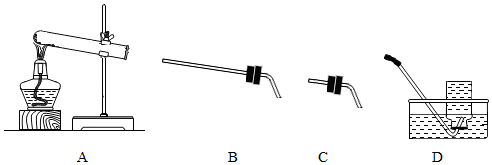
應選用的發生裝置組合是ACAC(填編號),用D裝置收集氧氣,當觀察到集氣瓶口出現大氣泡集氣瓶口出現大氣泡(現象)說明已集滿。收集完畢,將導管移出集氣瓶,再進行如下操作:
a.從水槽中取出集氣瓶
b.瓶口向上放置
c.在集氣瓶口蓋好毛玻璃片
正確的操作順序為cabcab(填字母順序);某同學用該方法收集的一瓶氧氣不純混有空氣,可能的原因是集氣瓶內未充滿水(或未出現連續氣泡就收集)集氣瓶內未充滿水(或未出現連續氣泡就收集)(寫一點)。下列裝置中的丙丙(填編號)也可以作為氧氣的收集裝置。
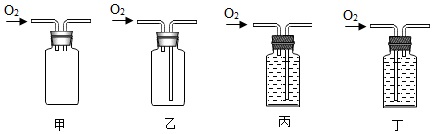
②B組同學用雙氧水、二氧化錳和如圖裝置進行實驗。
該方法制取氧氣的化學方程式是2H2O2 MnO2 2H2O+O2↑2H2O2 MnO2 2H2O+O2↑,組裝一套氧氣的發生和收集裝置有多種組合,除選擇儀器A、B和C外,還要從圖中選擇的儀器有DG或FHDG或FH(選填編號)。
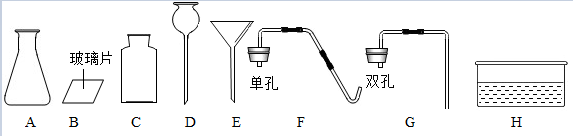
③氧氣的性質實驗:
鐵絲在氧氣中燃燒的化學方程式為3Fe+2O2 點燃 Fe3O43Fe+2O2 點燃 Fe3O4,實驗操作順序是badcbadc(用字母排序)。
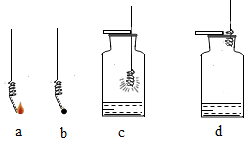
集氣瓶內預先留些水的作用是防止高溫熔融物濺落,炸裂瓶底防止高溫熔融物濺落,炸裂瓶底。
④思考與小結:
(1)氯酸鉀、雙氧水都能用于實驗室制取氧氣,因為它們都含有氧元素都含有氧元素。
(2)比較上述制取和收集氧氣的不同方法,歸納不正確的是cdcd(填編號)。
a.基本反應類型都屬于分解反應
b.選用的發生裝置不同是因為反應物的狀態、反應條件不同
c.用排空氣法收集氧氣驗滿的方法是將帶火星的木條伸入瓶內,若復燃則滿
d.能用排水法收集氧氣的依據是得到的氧氣較純凈
(3)使用藥品要節約,避免浪費。若要制取3瓶體積為200mL的氧氣,經過查閱相關資料并計算可知,這些氧氣的物質的量約為0.03mol。現在要制取0.03mol的氧氣,理論上需要氯酸鉀的質量為多少克?(根據方程式列式計算)
M
n
O
2
M
n
O
2
點燃
點燃
【答案】AC;集氣瓶口出現大氣泡;cab;集氣瓶內未充滿水(或未出現連續氣泡就收集);丙;2H2O2 2H2O+O2↑;DG或FH;3Fe+2O2 Fe3O4;badc;防止高溫熔融物濺落,炸裂瓶底;都含有氧元素;cd
M
n
O
2
點燃
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:100引用:1難度:0.9
相似題
-
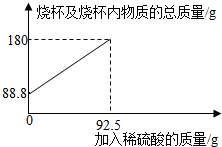 1.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入92.5g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
1.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入92.5g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
(1)該實驗取用的樣品質量為g。
(2)反應后所得溶液中的溶質的質量分數。(寫出計算過程,結果保留一位小數)
(3)反應結束后,小明不慎向燒杯中多加了10g稀硫酸,若在圖中補繪此過程中稀硫酸的質量與燒杯及燒杯內物質的總質量的關系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發布:2025/1/9 8:0:2組卷:4引用:1難度:0.3 -
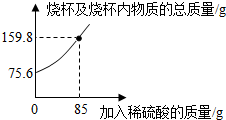 2.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為52.2g的燒杯中,然后緩慢加入一定質量的稀硫酸,當加稀硫酸質量為85g時,反應恰好完全(雜質不反應且產生的氣體全部逸出),反應過程中的質量關系如圖.完成下列問題:
2.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為52.2g的燒杯中,然后緩慢加入一定質量的稀硫酸,當加稀硫酸質量為85g時,反應恰好完全(雜質不反應且產生的氣體全部逸出),反應過程中的質量關系如圖.完成下列問題:
(1)該實驗取用的樣品質量為g.
(2)計算樣品中鐵的質量分數(寫出解題過程).發布:2025/1/9 8:0:2組卷:139引用:39難度:0.1 -
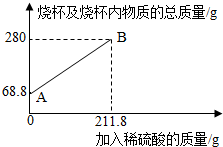 3.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入211.8g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
3.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入211.8g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
(1)該實驗取用的樣品質量為g。
(2)求樣品中鐵的質量分數;反應后所得溶液中的溶質的質量分數。(寫出計算過程,結果保留一位小數)
(3)反應結束后,小明不慎向燒杯中多加了20g稀硫酸,若在圖中補繪此過程中稀硫酸的質量與燒杯及燒杯內物質的總質量的關系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發布:2025/1/9 8:0:2組卷:8引用:1難度:0.3


