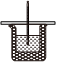
 實驗題:50mL0.50mol?L-1鹽酸與50mL0.55mol?L-1NaOH溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題:
實驗題:50mL0.50mol?L-1鹽酸與50mL0.55mol?L-1NaOH溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題:
(1)從實驗裝置上看,圖中缺少的一種玻璃儀器是 環形玻璃攪拌器環形玻璃攪拌器。
(2)寫出表示該反應中和熱的熱化學方程式(中和熱為57.3kJ?mol-1):H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ/molH+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ/mol(用離子方程式表示)。
(3)實驗中改用60mL0.50mol?L-1鹽酸與60mL0.55mol?L-1NaOH溶液進行反應,與上述實驗相比,所放出的熱量 不相等不相等(填“相等”或“不相等”),所求得的中和熱 相等相等(填“相等”或“不相等”)。
(4)用相同濃度和體積的氨水代替NaOH溶液進行上述實驗,測得的中和熱的數值會 偏小偏小(填“偏大””、“偏小””或“無影響”)。
(5)若三次平行操作測得數據中起始時鹽酸與燒堿溶液平均溫度相同,而終止溫度與起始溫度差(t2~t1)分別為①3.3℃、②3.5℃、③4.5℃,則最終代入計算式的溫差平均值為 3.43.4℃。計算該實驗測得的中和反應反應熱ΔH=-56.8kJ/mol-56.8kJ/mol(結果保留一位小數)[已知Q=cmΔt,設鹽酸和NaOH溶液的密度為1g/cm3,反應后混合溶液的比熱容(c)為4.18J/(g?℃)]。
【答案】環形玻璃攪拌器;H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ/mol;不相等;相等;偏小;3.4;-56.8kJ/mol
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/12/4 11:30:1組卷:60引用:3難度:0.6
相似題
-
1.在測定中和熱的實驗中,下列說法正確的是( )
A.在測定中和熱實驗中需要使用的儀器有:天平、量筒、燒杯、溫度計、玻璃棒 B.完成一次中和反應反應熱測定實驗,溫度計需要使用2次,分別用于測混合液的初始溫度和反應最高溫度 C.用50mL0.55mol/L的NaOH溶液與60mL0.50mol/L的鹽酸反應,測得的中和熱數值偏大 D.使用環形玻璃攪拌棒是為了使反應物充分混合減小實驗誤差 發布:2024/12/18 23:0:1組卷:88引用:2難度:0.7 -
2.下列說法正確的是( )
A.在鐵棒上鍍銅時,陽極不一定要用Cu做電極 B.反應NH3(g)+HCl(g)═NH4Cl(s)在室溫下可自發進行,則該反應的ΔH>0 C.中和熱測定實驗中,應把稀硫酸緩慢并分次倒入NaOH溶液中并攪拌 D.相同條件下,等pH的NaHSO4溶液和CH3COOH溶液,后者導電能力更強 發布:2024/10/21 1:0:2組卷:11引用:1難度:0.7 -
3.掌握化學實驗技能是進行科學探究的基本保證。下列有關說法正確的是( )

A.若將甲中注射器的活塞往右拉,能自動恢復到原位,說明甲裝置氣密性好 B.將甲虛線框中的裝置換為乙裝置,滴入稀硫酸后若注射器活塞右移,說明鋅與硫酸反應為放熱反應 C.用丙裝置進行中和反應反應熱的測定實驗時,NaOH要緩慢倒入稀硫酸中 D.丁裝置是排出堿式滴定管中的氣泡操作 發布:2024/12/17 3:0:1組卷:96引用:4難度:0.7


