鐵和鐵的化合物在工農業生產中有廣泛的應用。
(一)鐵的制備和防護
(1)人類向自然界索取量最大金屬的是鐵,高爐煉鐵時將鐵礦石粉碎的目的是 增大反應物的接觸面積,加快反應速率增大反應物的接觸面積,加快反應速率。
(2)鐵生銹的主要過程為: ,轉化③生成Fe2O3?xH2O,則x≤33(x為整數)。
,轉化③生成Fe2O3?xH2O,則x≤33(x為整數)。
(3)為防止鐵生銹,可對鐵制品進行“發藍”處理,使其表面生成致密氧化物(其中Fe、O元素質量比為21:8)保護膜,該氧化物的化學式為 Fe3O4Fe3O4。
(二)鐵的冶煉和探究
取2.40gFe2O3粉末,小組同學用如圖裝置模擬煉鐵,并測定反應后固體成分。(甲酸(HCOOH)在加熱、濃硫酸的作用下,分解生成CO和水)

(4)連接裝置,利用W型玻璃管進行實驗的優點 節約藥品節約藥品。
(5)控制A中溫度在800℃至固體全部變黑,繼續通CO至冷卻。
鐵的檢驗:將該微型裝置向右傾斜,使稀硫酸(濃硫酸吸收反應生成的水成為稀硫酸)流到A處,當看到 有氣泡產生有氣泡產生,證明有鐵生成。
(6)稱取0.720g水合草酸亞鐵晶體FeC2O4?2H2O,放在一個可稱量的敞口容器中高溫灼燒,容器中的固體質量如圖。
已知相對分子質量:FeC2O4?2H2O-180;CO-28;CO2-44;H2O-18

①200-300℃之間,分解產生的氣體為 水蒸氣水蒸氣。
②450℃時,固體主要成分是 氧化亞鐵氧化亞鐵。
③當溫度高于600℃,剩余固體質量略有增加的原因是 部分氧化亞鐵與空氣中的氧氣反應生成氧化鐵部分氧化亞鐵與空氣中的氧氣反應生成氧化鐵。
【答案】增大反應物的接觸面積,加快反應速率;3;Fe3O4;節約藥品;有氣泡產生;水蒸氣;氧化亞鐵;部分氧化亞鐵與空氣中的氧氣反應生成氧化鐵
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/7/1 8:0:9組卷:158引用:2難度:0.6
相似題
-
1.《天工開物》中描述了系統、連續的煉鐵煉鋼過程,利用煤炭煉鐵,從煉鐵爐流出的生鐵水,直接流進炒鐵爐里炒成熟鐵,從而減少了再熔化的過程。下列說法錯誤的是( )
A.煤炭燃燒的溫度能夠達到煉鐵所需的溫度 B.煉鐵爐中流出的是純鐵 C.生鐵炒成熟鐵的過程中降低了含碳量 D.該煉鐵工藝減少了再熔化的過程,節約燃料,彰顯了古代勞動人民的智慧 發布:2024/12/25 12:0:1組卷:287引用:4難度:0.9 -
2.在鋼鐵工業推進碳減排、碳捕集的過程中,化學發揮了重要作用。
(1)“焦炭煉鋼”是先將鐵精礦(Fe2O3)和焦炭同時加入高爐,鼓入熱空氣,充分反應后得到生鐵,再將生鐵轉移至煉鋼爐中煉制得鋼。
①高爐煉鐵的主要反應原理是在高溫下,奪取了Fe2O3里的氧將鐵還原出來。
②某鋼鐵廠每年需要向高爐中加入120萬噸的焦炭,若加入的焦炭全部轉化為CO2,則該鋼鐵廠每年排放CO2的質量為萬噸。
(2)為了實現CO2的捕集利用,我國研制出一種多功能復合催化劑(含Na-Fe3O4),能將CO2轉化為汽油,轉化步驟如下:
CO2COH2步驟Ⅰ(CH2)nH2步驟Ⅱ汽油步驟Ⅲ
①步驟Ⅰ除生成CO外,還生成另一種氧化物。該氧化物的化學式是。
②下列說法錯誤的是(填字母)。
a.所得汽油中含有C、H兩種元素
b.NaFe3O4中O為-2價,Fe為+3價
c.上述轉化不僅有利于CO2減排,還可以減輕人類對化石能源的需求
(3)一種以“氫能煉鋼”替代“焦炭煉鋼”的工藝流程如圖所示。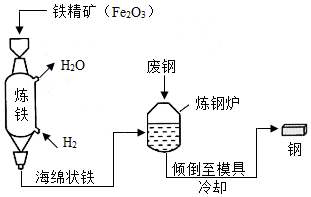
①高溫下,用H2煉鐵時反應的化學方程式為。
②跟“焦炭煉鋼”工藝相比,“氫能煉鋼”的主要優點有。
③從物質組成的角度,說明向煉鋼爐中加入廢鋼的目的:。發布:2024/12/25 15:30:1組卷:410引用:6難度:0.6 -
3.從1世紀起,鐵便成了一種最主要的金屬材料。

(1)上述三種鐵礦石的主要成分屬于氧化物的是。
(2)工業上用一氧化碳和赤鐵礦煉鐵的原理是(用化學方程式表示)。發布:2024/12/25 13:0:1組卷:31引用:4難度:0.5


