人類(lèi)通過(guò)海水資源的開(kāi)發(fā)和利用可以獲得許多有用的物質(zhì),以滿足我們生產(chǎn)生活的需要。以下為人類(lèi)利用海水獲得所需物質(zhì)的途徑,請(qǐng)回答以下相關(guān)問(wèn)題:
Ⅰ.分離淡水
(1)利用太陽(yáng)能將海水進(jìn)行蒸餾淡化的過(guò)程如下圖所示,淡化后淡水槽中得到的水屬于 軟水軟水(選填“硬水”或“軟水”)。

Ⅱ.提純海鹽
(2)海洋中含量最多的礦物是海鹽,即氯化鈉,人類(lèi)在海灘上建鹽田,通過(guò)貯水池、蒸發(fā)池和結(jié)晶池得到食鹽晶體和母液,此種結(jié)晶方法采用的原理是 利用陽(yáng)光和風(fēng)力使水分蒸發(fā),食鹽結(jié)晶出來(lái)利用陽(yáng)光和風(fēng)力使水分蒸發(fā),食鹽結(jié)晶出來(lái)。
Ⅲ.母液制鎂
將海鹽從海水中分離提純之后剩下的母液稱為苦鹵,其中含有許多有價(jià)值的元素,如鎂元素。目前從苦鹵(含有MgCl2)中提取金屬鎂的工藝流程圖如下:

(3)在苦鹵中倒入石灰乳,即可得到Mg(OH)2懸濁液,請(qǐng)寫(xiě)出該反應(yīng)的化學(xué)方程式:MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2。
(4)操作①的步驟為過(guò)濾,實(shí)驗(yàn)室過(guò)濾操作如圖,若過(guò)濾后濾液仍然渾濁,可能的原因是 濾紙破損濾紙破損。

(5)在沉淀物中加入稀鹽酸后即可得到MgCl2,該反應(yīng)屬于 復(fù)分解復(fù)分解反應(yīng) (填基本類(lèi)型)。
(6)通過(guò)電解熔融MgCl2使其分解,即可得到金屬鎂和氯氣,請(qǐng)寫(xiě)出該反應(yīng)的化學(xué)方程式:MgCl2 通電 Mg+Cl2↑MgCl2 通電 Mg+Cl2↑。
(7)在2000℃下用焦炭還原氧化鎂,也可以制得金屬鎂,但該方法的缺點(diǎn)是 該反應(yīng)條件要求苛刻,需要在較高的溫度下才能進(jìn)行該反應(yīng)條件要求苛刻,需要在較高的溫度下才能進(jìn)行。
通電
通電
【考點(diǎn)】對(duì)海洋資源的合理開(kāi)發(fā)與利用;濾液仍渾濁的原因;結(jié)晶的原理、方法及其應(yīng)用;硬水與軟水;反應(yīng)類(lèi)型的判定;書(shū)寫(xiě)化學(xué)方程式、文字表達(dá)式、電離方程式.
【答案】軟水;利用陽(yáng)光和風(fēng)力使水分蒸發(fā),食鹽結(jié)晶出來(lái);MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;濾紙破損;復(fù)分解;MgCl2 Mg+Cl2↑;該反應(yīng)條件要求苛刻,需要在較高的溫度下才能進(jìn)行
通電
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書(shū)面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/18 8:0:10組卷:74引用:2難度:0.5
相似題
-
1.閩東的淡水和海水資源豐富
(1)興趣小組測(cè)量集中水樣的pH,得到下表數(shù)據(jù),其中堿性最強(qiáng)的是(填序號(hào))
(2)山泉水含有較多鈣、鎂離子,硬度較高水樣 來(lái)源 pH A 泉水:“海上仙都”-太姥山 6.8~7.0 B 河水:“海國(guó)桃園”-楊家溪 7.2~7.6 C 海水:“天然良港”-三都澳 7.8~8.0
①寫(xiě)出鈣離子的符號(hào)
②若要降低其硬度,可采用的方法是(寫(xiě)一種)
(3)海水是重要資源,處理的大致流程如圖: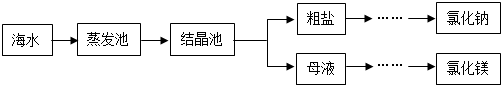
①粗鹽經(jīng)過(guò)溶解、過(guò)濾、蒸發(fā)可除去海沙等不溶性雜質(zhì).
a.海沙的主要成分是二氧化硅(SiO2),其中Si的化合價(jià)為.
b.若以上操作在實(shí)驗(yàn)室中進(jìn)行,溶解時(shí),玻璃棒的作用是.
②母液經(jīng)過(guò)處理,可得氯化鎂,點(diǎn)解熔融氯化鎂生成鎂和氯氣(Cl2).寫(xiě)出電解氯化鎂的化學(xué)方程式:.發(fā)布:2024/12/22 8:0:1組卷:13引用:1難度:0.5 -
2.我國(guó)的領(lǐng)海主權(quán)不容侵犯,南海是我國(guó)的固有領(lǐng)海,蘊(yùn)藏著豐富的海洋資源。
(1)南海不僅蘊(yùn)含著大量的煤、石油、天然氣等常規(guī)能源,還蘊(yùn)藏著大量的可燃冰。可燃冰(主要成分是CH4)被科學(xué)家譽(yù)為“未來(lái)能源”,CH4燃燒的化學(xué)方程式,可燃冰作為能源與煤、石油相比的優(yōu)點(diǎn)是。
(2)南海某島采用風(fēng)力發(fā)電提供的電能對(duì)海水進(jìn)行了如圖1所示的綜合利用。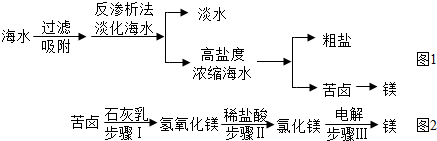
①反滲析法淡化海水是利用海水中各成分的不同分離出淡水。
②將高鹽度濃縮海水進(jìn)行可以分離得到粗鹽。
③用苦鹵制取金屬鎂的流程圖如圖2:
上述轉(zhuǎn)化過(guò)程中,所發(fā)生的反應(yīng)屬于復(fù)分解反應(yīng)類(lèi)型的步驟是(填序號(hào)),步驟Ⅱ的化學(xué)方程式為。利用苦鹵制取氫氧化鎂比“直接向海水中加入石灰乳制取氫氧化鎂”的優(yōu)勢(shì)是。
(3)如圖3是海水“制堿”的部分簡(jiǎn)單流程。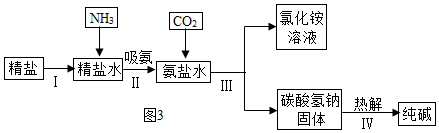
①步驟IⅡ反應(yīng)的化學(xué)方程式為;
②制氨鹽水的過(guò)程中要先通入氨氣,再通入二氧化碳,如果反過(guò)來(lái),二氧化碳的吸收率會(huì)降低,這是因?yàn)?!--BA-->;
③氨鹽水吸收二氧化碳后生成碳酸氫鈉和氯化銨,首先析出的物質(zhì)是,原因是,將氯化銨溶液和碳酸氫鈉固體分離的方法是過(guò)濾,濾液中的溶質(zhì)有。發(fā)布:2024/12/25 12:0:1組卷:85引用:4難度:0.6 -
3.海洋是人類(lèi)巨大的資源寶庫(kù),其中含有的可溶性物質(zhì)包括MgCl2等。如圖為從海水中提取金屬鎂的簡(jiǎn)易流程圖。

(1)海洋中含量最多的物質(zhì)是。
(2)貝殼煅燒的化學(xué)方程式是。
(3)操作Ⅰ的名稱是,進(jìn)行該操作時(shí),用到的玻璃儀器有燒杯、玻璃棒和。其中玻璃棒的作用是。
(4)生石灰轉(zhuǎn)化為石灰乳的過(guò)程是反應(yīng)(選填“吸熱”或“放熱”)。
(5)寫(xiě)出氫氧化鎂和鹽酸反應(yīng)的化學(xué)方程式。
(6)上述流程中未涉及到的基本反應(yīng)類(lèi)型是反應(yīng)。發(fā)布:2024/12/24 12:0:2組卷:221引用:4難度:0.2
相關(guān)試卷


