小明同學欲通過實驗證明“二氧化錳是氯酸鉀受熱分解的催化劑”這一命題。他設計并完成了下表所示的探究實驗:
|
實驗操作 |
實驗現象 |
實驗結論或總結 | ||
| 各步驟結論 | 總結 | |||
|
實驗一 |
將氯酸鉀加熱至熔化,伸入帶火星的木條。 |
木條復燃 |
氯酸鉀受熱要分解產生氧氣,反應的文字(或符號)表達式為: ① 氯酸鉀 加熱 △ 氯酸鉀 加熱 △ |
二氧化錳是氯酸鉀受熱分解的催化劑 |
|
實驗二 |
將二氧化錳加熱至熔化,伸入帶火星的木條。 |
② 無明顯現象 無明顯現象 |
二氧化錳受熱不產生氧氣 |
|
| 實驗三 | ③ 將氯酸鉀和二氧化錳混合后加熱,伸入帶火星的木條 將氯酸鉀和二氧化錳混合后加熱,伸入帶火星的木條 |
木條迅速復燃 | 二氧化錳能加快氯酸鉀的分解 | |
(2)在小明同學不同的探究實驗中,實驗一和實驗二起的作用是
實驗一的作用是加熱至較高溫度時氯酸鉀才能夠分解;實驗二的作用是加熱至較高溫度時二氧化錳不能分解
實驗一的作用是加熱至較高溫度時氯酸鉀才能夠分解;實驗二的作用是加熱至較高溫度時二氧化錳不能分解
。(3)小明同學繼續探究二氧化錳用量對反應速率影響,他們做了這樣一組實驗:每次用30mL10%過氧化氫溶液,采用不同量二氧化錳粉末做實驗,測定各收集到500mL氧氣的所用時間結果如下:(其他實驗條件均相同)
| 實驗次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 二氧化錳用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 時間(秒) | 22 | 13 | 12 | 10 | 9 | 8 | 5 | 3 | 3 | 3 |
一定范圍內隨著二氧化錳質量的增加,過氧化氫的分解速率加快;一定范圍內隨著二氧化錳質量的增加,反應速率不變
一定范圍內隨著二氧化錳質量的增加,過氧化氫的分解速率加快;一定范圍內隨著二氧化錳質量的增加,反應速率不變
。(5)拓展:催化劑在工業上應用較多。工業上用氫氣和氮氣在高溫及催化劑的條件下合成氨氣(NH3)。請仔細觀察如圖所示,
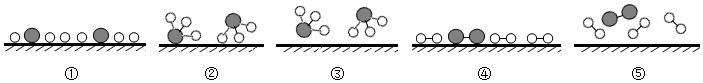 寫出符合二者在該條件下的文字(或符號)表達式:
寫出符合二者在該條件下的文字(或符號)表達式:氮氣+氫氣氨氣或N2+H2NH3
催化劑
高溫
催化劑
高溫
氮氣+氫氣氨氣或N2+H2NH3
,其基本反應類型:催化劑
高溫
催化劑
高溫
化合反應
化合反應
。【考點】催化劑的特點與催化作用.
【答案】氯酸鉀氯化鉀+氧氣或KClO3KCl+O2;無明顯現象;將氯酸鉀和二氧化錳混合后加熱,伸入帶火星的木條;實驗一的作用是加熱至較高溫度時氯酸鉀才能夠分解;實驗二的作用是加熱至較高溫度時二氧化錳不能分解;一定范圍內隨著二氧化錳質量的增加,過氧化氫的分解速率加快;一定范圍內隨著二氧化錳質量的增加,反應速率不變;氮氣+氫氣氨氣或N2+H2NH3;化合反應
加熱
△
催化劑
高溫
催化劑
高溫
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:26引用:1難度:0.5
相似題
-
1.下列有關催化劑的說法正確的是( )
A.化學反應前后催化劑的化學性質通常會發生改變 B.在化學反應中催化劑只能加快物質的反應速率 C.催化劑只能改變化學反應速率,不能增加或減少生成物的質量 D.要使過氧化氫溶液分解出氧氣必須加入二氧化錳,否則就不能發生分解反應 發布:2024/12/25 11:0:2組卷:65引用:3難度:0.5 -
2.用過氧化氫溶液制取氧氣時,忘記加二氧化錳,其結果是( )
A.不放出氧氣 B.放出氧氣總量會減少 C.放出氧氣速率慢 D.放出氧氣總量更多 發布:2024/12/25 11:30:2組卷:16引用:2難度:0.7 -
3.“忽如一夜春風來,千樹萬樹梨花開”.今年2月18日入夜,經過千余名人工增雨作業人員的奮力鏖戰,天人戮力,一場久違的大雪降臨河北大地,給這方焦渴的土地帶來了生機和希望.其原理就是使用催化劑使云中的小水滴相互凝結,形成降雨(雪).目前,人工增雨使用的催化劑通常分為三類:第一類是可以大量產生凝結核或凝華核的碘化銀等成核劑;碘化銀(AgI)在高溫下瞬間分解生成銀單質和碘單質(I2)形成人工冰核使水汽凝聚形成冰晶.第二類是可以使云中的水分形成大量冰晶的干冰、液氮等制冷劑.第三類是可以吸附云中水分變成較大水滴的鹽粒等吸濕劑.
(1)下面關于這些催化劑描述不正確的是.
A.干冰是氧化物
B.液氮是綠色增雨劑對環境無污染
C.在增雨過程中液氮和干冰只發生了物理變化
D.液氮是一種溶液,降落的雨滴中將含有大量的液氮
(2)寫出碘化銀分解的化學方程式.
(3)干冰和液氮可以使云中的水分形成大量冰晶的原理是.發布:2025/1/4 8:0:1組卷:8引用:1難度:0.7


