“化學反應條件的控制是實驗靈魂”。小強同學欲通過實驗證明“二氧化錳是過氧化氫分解的催化劑”這一命題。請回答下列問題:
(1)取兩支大試管,分別倒入適量的5%、15%的過氧化氫溶液,再加入等量的MnO2,各收集一小試管氣體,發(fā)現(xiàn)濃度大的先收集滿。該操作過程中合理的順序是 ①③⑤④②①③⑤④②(選填序號)。
①檢驗裝置的氣密性
②有連續(xù)穩(wěn)定氣泡再排水集氣
③將水槽中待收集氣體的小試管注滿水
④旋緊連有導管的單孔塞
⑤向大試管內(nèi)倒入適量過氧化氫溶液再加入少許MnO2粉末
(2)他設(shè)計并完成了下表所示的探究實驗:
| 實驗操作 | 實驗現(xiàn)象 | 實驗結(jié)論 | 實驗總結(jié) | |
| 實驗一 | 取10mL8%的過氧化氫溶液于試管中,伸入帶火星的木條 | 有氣泡產(chǎn)生,木條不復燃 | 過氧化氫分解產(chǎn)生氧氣,反應速率 較慢 較慢 (填“較快”或“較慢”) |
二氧化錳是過氧化氫分解的催化劑 |
| 實驗二 | 向盛水的試管中加入二氧化錳,伸入帶火星的木條 | 沒有明顯現(xiàn)象 |
二氧化錳不能與水作用產(chǎn)生氧氣 二氧化錳不能與水作用產(chǎn)生氧氣
|
|
| 實驗三 |
取10mL8%的過氧化氫溶液于試管中,加入二氧化錳,伸入帶火星的木條 取10mL8%的過氧化氫溶液于試管中,加入二氧化錳,伸入帶火星的木條
|
有氣泡產(chǎn)生,木條復燃 有氣泡產(chǎn)生,木條復燃
|
二氧化錳能加快過氧化氫的分解 |
對比作用(合理即可)
對比作用(合理即可)
。2.小芳同學認為僅由上述實驗還不能完全得出表內(nèi)的“實驗總結(jié)”,她補充設(shè)計了兩個方面的探究實驗,最終完成了對“命題”的實驗證明。
①對二氧化錳進行了兩次稱量,其目的是
探究反應前后二氧化錳的質(zhì)量是否改變
探究反應前后二氧化錳的質(zhì)量是否改變
。②倒掉實驗三反應后的液體,向剩余的固體中重新加入過氧化氫溶液,反復實驗,其目的是
探究反應前后二氧化錳的化學性質(zhì)是否改變
探究反應前后二氧化錳的化學性質(zhì)是否改變
。【答案】①③⑤④②;較慢;二氧化錳不能與水作用產(chǎn)生氧氣;取10mL8%的過氧化氫溶液于試管中,加入二氧化錳,伸入帶火星的木條;有氣泡產(chǎn)生,木條復燃;對比作用(合理即可);探究反應前后二氧化錳的質(zhì)量是否改變;探究反應前后二氧化錳的化學性質(zhì)是否改變
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/10/18 9:0:1組卷:110引用:5難度:0.5
相似題
-
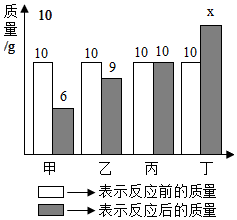 1.甲、乙、丙、丁四種物質(zhì)在反應前后的質(zhì)量關(guān)系如圖所示,下列有關(guān)說法錯誤的是( )
1.甲、乙、丙、丁四種物質(zhì)在反應前后的質(zhì)量關(guān)系如圖所示,下列有關(guān)說法錯誤的是( )A.x的值是15 B.丙可能是該反應的催化劑 C.丁是反應物 D.參加反應的甲和乙的質(zhì)量比為4:1 發(fā)布:2024/8/9 8:0:9組卷:54引用:4難度:0.7 -
2.在密閉容器中加入甲、乙、丙、丁四種物質(zhì),使之充分反應,反應前后測得有關(guān)數(shù)據(jù)如表:
下列說法中,不正確的是( )物質(zhì) 甲 乙 丙 丁 反應前質(zhì)量/g 18 1 2 32 反應后質(zhì)量/g X 26 2 12 A.反應后物質(zhì)甲的質(zhì)量為13g B.該反應的類型是分解反應 C.反應中乙、丁的質(zhì)量比為5:4 D.丙可能是該反應的催化劑 發(fā)布:2024/8/31 3:0:11組卷:45引用:4難度:0.4 -
3.一定條件下,甲、乙、丙、丁、戊五種物質(zhì)在密閉容器中發(fā)生反應,反應一段時間后,測得反應前后各種物質(zhì)的質(zhì)量(單位:g)如圖所示,下列說法不正確的是( )
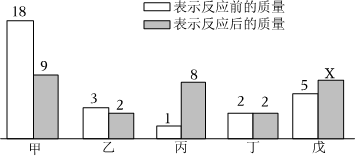 ?
?A.x的數(shù)值為8 B.丁可能是該反應的催化劑 C.反應前后乙、丙變化的質(zhì)量之比為1:7 D.該反應一定是復分解反應 發(fā)布:2024/8/3 8:0:9組卷:12引用:1難度:0.5
相關(guān)試卷


