冬天下大雪時,小華看到護路工人往路面撒上大量的鹽,他了解到道路結冰會對行車安全造成危害,撒鹽可以使路面的冰雪熔化。小華不禁產生了疑問,在相同的氣溫下,為什么撒了鹽后的冰就會熔化呢?

(1)小華回家后進行了探究,他從冰箱里取出一些冰塊,分別放入甲、乙兩個相同的易拉罐中,并在乙罐中加入適量的鹽,用筷子攪拌一段時間(如圖1)。當兩罐內 混合物處于固液共存狀態混合物處于固液共存狀態時,用溫度計分別測出罐內混合物的溫度(示數如圖2),乙罐中混合物的溫度為 零下6℃零下6℃,對比甲罐溫度小華得出相同的氣溫下撒了鹽后的冰會熔化的原因是 鹽降低了冰的熔點鹽降低了冰的熔點。
(2)小華還發現,一只罐外壁出現了白霜,而另一只外壁出現的是小水珠,出現白霜的是 乙乙(選填“甲”或“乙”)罐。
【考點】熔點與凝固點的影響因素;凝華的概念及現象.
【答案】混合物處于固液共存狀態;零下6℃;鹽降低了冰的熔點;乙
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/8/3 8:0:9組卷:879引用:8難度:0.5
相似題
-
1.在北方的冬天,汽車駕駛員常用水和酒精的混合物作為汽車冷卻系統的冷卻劑,這是由于這種混合液具有( )
A.較低的沸點 B.較高的熔點 C.較低的凝固點 D.較好的冷卻效果 發布:2024/9/24 2:0:8組卷:794引用:4難度:0.9 -
2.小明結合剛剛學過的物理知識對汽車進行了一系列的研究。他發現加入防凍液后的混合液冬天不容易凝固,長時間開車也不容易沸騰。
有關資料表明,防凍液與水按不同的比例混合,混合液的凝固點不同,具體數值參見下表。防凍液含量/%(體積比) 30 40 50 60 70 80 90 混合液的凝固點/℃ -17 -28 -32 -49 -48 -46 -28 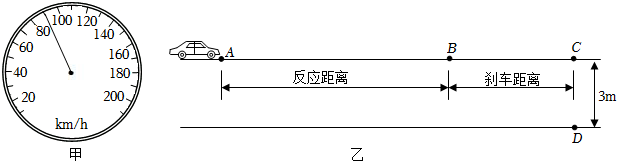 ?
?
(1)在混合液中,如果防凍液含量由30%逐漸增大到90%,則混合液凝固點的變化情況是 。
A.逐漸升高
B.逐漸降低
C.先升高后降低
D.先降低后升高
(2)汽車勻速行駛時速度表顯示如圖甲所示,汽車速度為 km/h。
(3)小明了解到人在飲酒后駕車的應急反應時間是未飲酒時的2~3倍,反應時間是指司機從看到意外情況到踩剎車需要的這段時間,在反應時間內汽車要保持原速前進一段距離,這段距離叫反應距離;剎車后汽車由于慣性還要繼續行駛一段距離,這段距離稱為剎車距離。
若某司機飲酒后駕車以圖甲所示速度沿馬路直線行駛,如圖乙所示,在A點發現前方危險情況(一行人正從路邊距離C點3m的D點橫穿馬路),在B點踩剎車,在C點完全停下,共用時3s(經過反應時間和剎車時間),一共行駛了48m,已知剎車過程的平均速度為2.5m/s,則:
①求這輛汽車從A點發現情況到剎住車后停在C點的平均速度;
②求該司機飲酒后的反應時間;
③若行人以1.3m/s的速度行走,請計算說明汽車是否有撞上行人的可能?(提示:該車的寬度約1.8m;車身接觸到行人即為相撞)發布:2024/9/27 2:0:1組卷:36引用:1難度:0.6 -
3.在北方的冬天,汽車的駕駛員常把水和酒精的混合物作為汽車冷卻系統中的冷卻液,這是因為這種冷卻液具有( )
A.較高的熔點 B.較低的凝固點 C.較低的沸點 D.更容易蒸發 發布:2024/10/25 3:0:4組卷:189引用:3難度:0.5


