 常溫下,將除去表面氧化膜的Al、Cu片插入電解質A溶液中組成原電池,如圖所示:
常溫下,將除去表面氧化膜的Al、Cu片插入電解質A溶液中組成原電池,如圖所示:
(1)若A為稀鹽酸,則Al片作 負負極,該電極的電極反應式為 Al-3e-═Al3+Al-3e-═Al3+。
(2)若A為NaOH,則Al片作 負負極,該電極的電極反應式為 Al+4OH--3e-═AlO-2+2H2OAl+4OH--3e-═AlO-2+2H2O。
(3)若A為稀HNO3,則Cu片作 正正極。
A
l
O
-
2
A
l
O
-
2
【考點】原電池原理.
【答案】負;Al-3e-═Al3+;負;Al+4OH--3e-═+2H2O;正
A
l
O
-
2
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:118引用:3難度:0.7
相似題
-
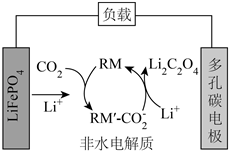 1.我國某科研團隊借助氧化還原介質RM,將Li-CO2電池的放電電壓提高至3V以上,該電池的工作原理如圖。下列說法正確的是( )
1.我國某科研團隊借助氧化還原介質RM,將Li-CO2電池的放電電壓提高至3V以上,該電池的工作原理如圖。下列說法正確的是( )A.LiFePO4電極的電勢比多孔碳電極的高 B.負極反應:LiFePO4-xe-═Li(1-x)FePO4+xLi+ C.RM和RM′- 均為該電池反應的催化劑CO-2D.LiFePO4電極每減重7g,就有22gCO2被固定 發布:2024/12/20 4:30:1組卷:157引用:2難度:0.5 -
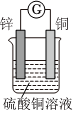 2.如圖所示將鋅、銅通過導線相連,置于硫酸銅溶液中。
2.如圖所示將鋅、銅通過導線相連,置于硫酸銅溶液中。
(1)該裝置將轉化為能。
(2)Zn電極為極,發生反應,電極方程式為。
(3)外電路電子由電極經導線流向電極。
(4)若反應過程中鋅溶解了6.5g,則銅電極增重g,該回路中轉移的電子數為。發布:2024/12/30 3:0:4組卷:316引用:2難度:0.7 -
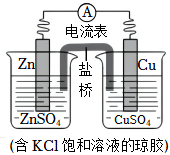 3.銅鋅原電池的裝置如圖,其中鹽橋為內含KCl的瓊脂凝膠,下列說法不正確的是( )
3.銅鋅原電池的裝置如圖,其中鹽橋為內含KCl的瓊脂凝膠,下列說法不正確的是( )A.Zn是負極反應物,發生氧化反應 B.電子從鋅片流向銅片 C.銅電極上發生反應Cu2++2e-═Cu D.鹽橋中Cl-進入CuSO4溶液 發布:2024/12/15 19:30:1組卷:195引用:1難度:0.5


