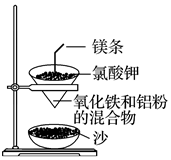
 鋁熱反應原理可以應用在生產上,如用于焊接鋼軌等,實驗室鋁熱反應的實驗裝置如圖所示。
鋁熱反應原理可以應用在生產上,如用于焊接鋼軌等,實驗室鋁熱反應的實驗裝置如圖所示。
(1)該實驗步驟如下:用兩張圓形濾紙分別折疊成漏斗狀,套在一起,使四周都是四層。把內層漏斗取出,在底部剪一個孔,用水潤濕,再跟另一個漏斗套在一起,架在鐵圈上,下面放置盛沙的蒸發皿蒸發皿(填儀器名稱)。把5g炒干的氧化鐵粉末和2g鋁粉混合均勻,放在漏斗中,上面加少量氯酸鉀,并在混合物中間插一根鎂條,用小木條點燃鎂條,觀察發生的現象。
(2)圖中漏斗的材質是紙質紙質(填“玻璃”或“紙”)。
(3)鎂條的作用是利用鎂條燃燒放出的熱量促使氧化鐵和鋁發生劇烈反應利用鎂條燃燒放出的熱量促使氧化鐵和鋁發生劇烈反應。
(4)實驗現象有:
①鎂條劇烈燃燒鎂條劇烈燃燒;
②反應劇烈,放出大量的熱,發出耀眼的光芒反應劇烈,放出大量的熱,發出耀眼的光芒;
③紙漏斗的下部被燒穿,有熔融物落下紙漏斗的下部被燒穿,有熔融物落下。
(5)待熔融物冷卻后,除去外層熔渣,仔細觀察,可以發現落下的是鐵鐵珠。
(6)寫出該反應的化學方程式:2Al+Fe2O3 高溫 Al2O3+2Fe2Al+Fe2O3 高溫 Al2O3+2Fe;在冶金工業上也常用這一反應原理來冶煉DD(填字母)。
A.不活潑金屬
B.較活潑金屬
C.稀有金屬
D.高熔點金屬
高溫
高溫
【考點】探究鋁熱反應.
【答案】蒸發皿;紙質;利用鎂條燃燒放出的熱量促使氧化鐵和鋁發生劇烈反應;鎂條劇烈燃燒;反應劇烈,放出大量的熱,發出耀眼的光芒;紙漏斗的下部被燒穿,有熔融物落下;鐵;2Al+Fe2O3 Al2O3+2Fe;D
高溫
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:14引用:3難度:0.7
相似題
-
 1.按要求回答下列問題:
1.按要求回答下列問題:
(1)實驗室鋁粉和Fe2O3作鋁熱反應實驗,鋁熱反應的方程式為,該實驗中除用到鋁粉和Fe2O3外,需要的試劑還有(填編號).
a.KClO3 b.Mg c.MnO2 d.KCl
(2)據文獻報道,在實際反應中鋁熱反應的產物成分較為復雜.某課題組對鋁熱反應產物的成分進行探究,經成分分析,發現主要得到甲和乙兩種產物.甲由具有相同電子層結構的陰、陽離子構成;乙是一種鐵鋁的金屬互化物(可用FexAly表示),取該合金粉末2.47g,滴加足量濃NaOH溶液,充分攪拌、過濾、洗滌得固體.再將所得固體在空氣中充分加熱、灼燒得紅棕色粉末1.60g.
①甲的化學式為,乙中x=,y=.
②甲的晶體是耐高溫材料,用此材料做成的坩堝,不能用來熔融NaOH,用化學方程式解釋其原因;
含二氧化硅材料做成的坩堝(填“能”或“不能”)用來熔融NaOH.
③如圖表示室溫下相同組分的乙分別在兩種不同的酸中的腐蝕情況,由圖可知,乙在中具有比較強的抗腐蝕性,原因可能是.
④研究發現鋁熱反應后期溫度高達2000℃以上時會有極微量的Al4C3生成,Al4C3遇水會產生一種氣體,該氣體的分子式為.[已知CaC2+2H2O═Ca(OH)2+C2H2↑]
(3)鎂鋁互化物(Mg17Al12)是一種潛在的貯氫材料,該金屬互化物在一定條件下完全吸氫的反應方程式為Mg17Al12+17H2═17MgH2+12Al.得到的混合物在6.0mol?L-1HCl中,能完全釋放出H2.1mol Mg17Al12完全吸氫后得到的混合物與上述鹽酸完全反應,釋放出H2的物質的量為.發布:2024/12/6 8:0:2組卷:24引用:1難度:0.3 -
2.“鋁熱反應”是一種重要的化學反應,下列說法正確的是( )
A.是吸熱反應 B.鋁熱劑是純凈物 C.鋁熱劑是混合物 D.鋁熱反應不是氧化還原反應 發布:2025/1/21 8:0:1組卷:48引用:1難度:0.9 -
3.下列關于鋁熱反應的說法錯誤的是( )
A.鋁熱反應中的還原劑是鋁粉 B.鋁熱劑是純凈物 C.鋁與Fe2O3可組成鋁熱劑 D.鋁熱反應是放熱反應 發布:2025/1/21 8:0:1組卷:13引用:3難度:0.6


