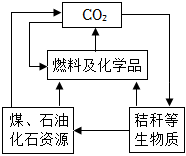
煤是社會生產、生活中最重要的能源,其主要成分是碳。工業上常把煤進行氣化和液化處理,使煤變成清潔能源。煤氣化和液化流程示意圖如圖
(1)粗煤屬于混合物混合物(填“純凈物”或“混合物”);第①步操作發生的是物理物理(填“物理”或“化學”)變化。
(2)第②步是精煉煤與水蒸氣的反應,化學方程式為C+H2O 高溫 CO+H2C+H2O 高溫 CO+H2。
(3)第③步通過化合反應得到一種有機燃料甲醇(CH3OH),該過程的化學方程式為CO+2H2 催化劑 CH3OHCO+2H2 催化劑 CH3OH,該反應中CO與H2的質量比為7:17:1。
(4)上述流程中產生的SO2,若直接排放到空氣中會導致酸雨。酸雨的形成過程如下:
SO2+H2O=X,2X+O2=2H2SO4,則X的化學式為H2SO3H2SO3。
(5)從“綠色化學”的角度分析,“煤的氣化和煤的液化”生產流程的優點是原料全部轉化為產品或實現“零排放”,不對環境造成污染。原料全部轉化為產品或實現“零排放”,不對環境造成污染。。
高溫
高溫
催化劑
催化劑
【答案】混合物;物理;C+H2O CO+H2;CO+2H2 CH3OH;7:1;H2SO3;原料全部轉化為產品或實現“零排放”,不對環境造成污染。
高溫
催化劑
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:57引用:2難度:0.7