鉻鐵礦主要成分為FeO?Cr2O3,含有SiO2、Al2O3等雜質。工業上用鉻鐵礦制備紅礬鈉(Na2Cr2O7)的流程如圖所示:煅燒時反應為:4FeO?Cr2O3+7O2+20NaOH 煅燒 8Na2CrO4+4NaFeO2+10H2O

(1)步驟①是在坩堝中進行煅燒,可用作此坩堝材料的是AA。
A.鐵 B.氧化鋁 C.石英 D.陶瓷
(2)步驟①煅燒反應極慢,需要升溫至NaOH呈熔融狀態,反應速率才加快,其原因為熔融后增大了反應物的接觸面積熔融后增大了反應物的接觸面積。
(3)步驟②中NaFeO2會強烈水解生成氫氧化鐵沉淀,其化學方程式為NaFeO2+2H2O=Fe(OH)3↓+NaOHNaFeO2+2H2O=Fe(OH)3↓+NaOH。
(4)將五份濾液1分別在130℃蒸發1小時,各自冷卻到不同溫度下結晶,保溫過濾,所得實驗數據如下表。根據數據分析,步驟③的最佳結晶溫度為4040。
煅燒
| 結晶溫度/℃ | Na2CrO4粗晶中各物質含量/w% | |||
| Na2CrO4?4H2O | NaOH | Na[Al(OH)4] | Na2SiO3 | |
| 30 | 52.45 | 29.79 | 8.69 | 12.21 |
| 40 | 68.81 | 20.49 | 8.46 | 10.84 |
| 50 | 60.26 | 27.96 | 10.36 | 9.32 |
| 60 | 50.74 | 29.66 | 10.40 | 12.25 |
| 70 | 46.77 | 33.06 | 8.10 | 6.48 |
Al(OH)3、H2SiO3(或H4SiO4)
Al(OH)3、H2SiO3(或H4SiO4)
。(6)假設該流程中鉻元素完全轉化為紅礬鈉,則該鉻鐵礦中鉻元素的質量分數為
52
m
2
131
m
1
52
m
2
131
m
1
【答案】A;熔融后增大了反應物的接觸面積;NaFeO2+2H2O=Fe(OH)3↓+NaOH;40;Al(OH)3、H2SiO3(或H4SiO4);
52
m
2
131
m
1
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:63引用:3難度:0.3
相似題
-
1.我國青藏高原的鹽湖中蘊藏著豐富的鋰資源,已探明的儲量約三千萬噸,碳酸鋰制備高純金屬鋰的一種工藝流程如圖。下列有關說法錯誤的是( )
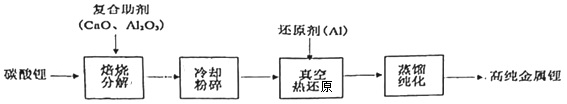
A.金屬鋰可保存在煤油中 B.使用復合助劑有利于碳酸鋰的分解 C.“粉碎”是為了增加接觸面積,加快反應速率 D.真空熱還原發生的主要化學反應為2Al+3Li2O 6Li+Al2O3高溫發布:2025/1/6 7:30:5組卷:28引用:2難度:0.9 -
2.硫鐵礦燒渣是硫鐵礦生產硫酸過程中產生的工業廢渣(主要含Fe2O3及少量SiO2、Al2O3等雜質)。用該燒渣制取藥用輔料-紅氧化鐵的工藝流程如圖:
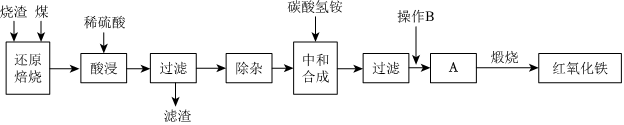
(1)在“還原焙燒”中產生的有毒氣體可能有。
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示)。
(3)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則操作B是。
(4)煅燒A的反應方程式是。
(5)ag燒渣經過上述工藝可得紅氧化鐵bg。藥典標準規定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質量分數應不低于(用含a、b的表達式表示)。發布:2025/1/19 8:0:1組卷:30引用:1難度:0.5 -
3.查閱資料:CaO、MgO在高溫下與C難反應,但能與SiO2反應.硫鐵礦燒渣是一種工業廢渣(含Fe2O3及少量SiO2、Al2O3、CaO、MgO等雜質),該燒渣可用于制取氧化鐵,具體化工生產工藝流程如下:
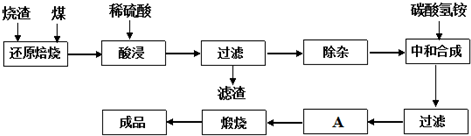
(1)焙燒時產生的主要有害氣體是.
(2)若在空氣中“酸浸”時間過長,溶液中Fe2+含量將下降,其原因是:(用離子方程式表示).
(3)根據下表數據:
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,檢驗Fe3+已經除盡的試劑是(除KSCN外).
(4)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則A的操作是.發布:2025/1/19 8:0:1組卷:12引用:1難度:0.1


