歸納與演繹是重要的科學方法,也是常用的科學學習方法。
(1)我們已經學習過實驗室制取O2、CO2兩種氣體的反應原理、制取與收集方法。請你歸納出實驗室制取氣體反應的共同點 ③⑤③⑤(填序號,可多選)
①需要加熱②使用催化劑③沒有氣體參加反應④原料為純凈物⑤只生成一種氣體
如圖是實驗室常見的制取和收集氣體的裝置圖,請回答下列問題:

(2)寫出如圖中指定序號的儀器名稱:③長頸漏斗長頸漏斗④集氣瓶集氣瓶;寫出儀器②的一種用途 給反應加熱給反應加熱。
(3)科學上可以通過多種反應生成氨氣(化學式為NH3,極易溶于水,密度比空氣小):
①2NH4Cl(固)+Ca(OH)2(固) △ CaCl2+2NH3↑+2H2O
②CaO(固)+NH3?H2O(濃)═NH3↑+Ca(OH)2
若在實驗室制取氨氣,我將選擇反應 ①①(只寫一個,填字母)。相應需要選用上面裝置圖中的 BB來作氣體發生裝置(連接裝置已經省略),選用 DD作為收集裝置。
(4)某研究小組對用雙氧水分解生成水和氧氣的實驗條件進行探究,完成了以下實驗:
①往盛有5mL5%H2O2溶液的試管中,伸入帶火星的木條,木條不復燃。
②往盛有5mLw%H2O2溶液的試管中,加入agMnO2,伸入帶火星的木條,木條復燃。
③往盛有5mLw%H2O2溶液的試管中,加入agFe2O3,伸入帶火星的木條,木條復燃。
④經檢驗,②③中反應后試管中仍分別含有agMnO2和agFe2O3
問題一:請寫出用雙氧水和二氧化錳制氧氣的化學反應方程式 2H2O2 MnO2 2H2O+O2↑2H2O2 MnO2 2H2O+O2↑。
問題二:MnO2和Fe2O3在上述反應中的作用是 催化作用催化作用。
實驗②③中的H2O2的濃度(w%)以 5%5%為宜。
(5)若制取氧氣1.6克,需10%的H2O2溶液多少克?(可能用到的相對原子質量:H-1O-16)
△
M
n
O
2
M
n
O
2
【答案】③⑤;長頸漏斗;集氣瓶;給反應加熱;①;B;D;2H2O2 2H2O+O2↑;催化作用;5%
M
n
O
2
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:3引用:1難度:0.7
相似題
-
 1.紹興盛產一種四角菱,稱“馱背白”。其菱肉富含淀粉等多種營養物質,此外菱角的莖和根富含纖維素(C6H10O5)n,也是一種很不錯的食物和藥材。
1.紹興盛產一種四角菱,稱“馱背白”。其菱肉富含淀粉等多種營養物質,此外菱角的莖和根富含纖維素(C6H10O5)n,也是一種很不錯的食物和藥材。
(1)菱肉中的鈣、磷、鐵等元素是以(填“單質”或“化合物”)的形態存在;
(2)該纖維素中C、H、O元素的質量比(最簡比);
(3)查閱資料獲悉菱肉制成的菱粉質細爽滑,為淀粉中之佳品。求菱葉產生3.6千克淀粉[有機物(CH2O)n]的同時,光合作用產生氧氣多少千克?(已知光合作用的化學方程式為:nCO2+nH2O═(CH2O)n+nO2,條件忽略)發布:2025/1/6 8:0:1組卷:4引用:1難度:0.5 -
2.小金為測定某樣品中氧化銅的質量分數,稱量固體樣品20.0克,用如圖所示的裝置進行實驗(雜質不參與反應且生成水完全被吸收),實驗中共消耗0.6克氫氣,測得B裝置反應前后的質量增加了3.6克。
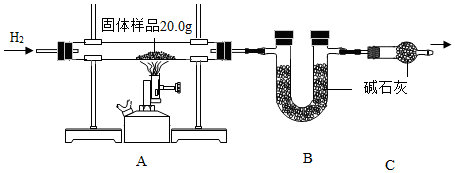
(1)C裝置的作用是;
(2)計算固體樣品中氧化銅的質量分數(根據化學方程式列式計算)。發布:2024/12/28 15:30:1組卷:12引用:2難度:0.5 -
3.侯德榜是我國著名的化學家,發明了侯氏制堿法,其反應原理如下:NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl,請回答:
(1)反應產物中NH4C1可以用于農業生產,它屬于化肥中的肥。
(2)生產16.8t碳酸氫鈉,理論上需要氯化鈉的質量是多少?發布:2024/12/28 15:30:1組卷:12引用:2難度:0.5


