 Ⅰ、某班在實驗室進行制取乙酸乙酯的分組實驗,主要步驟如下:
Ⅰ、某班在實驗室進行制取乙酸乙酯的分組實驗,主要步驟如下:
①按如圖連接好裝置,并檢查裝置的氣密性。
②在試管甲中加入3mL乙醇,然后邊振蕩試管邊慢慢加入2mL濃硫酸和2mL乙酸,再加入沸石。然后用酒精燈緩慢加熱。
③待試管乙(裝有少量飽和碳酸鈉溶液)中收集到一定量產(chǎn)物后停止加熱,撤出試管B,振蕩后靜置。
已知:
| 相對分子質(zhì)量 | 密度/(g?cm -3) | 熔點/℃ | 沸點/℃ | 水中溶解性 | |
| 乙醇 | 46 | 0.789 | -117.3 | 78.5 | 以任意比互溶 |
| 乙酸 | 60 | 1.050 | 16.6 | 117.9 | 易溶 |
| 乙酸乙酯 | 88 | 0.897 | -84 | 77 | 難溶 |
(1)試管甲中主要反應(yīng)的化學(xué)方程式為
CH3COOH+C2H5OH CH3COOCH2CH3+H2O
濃硫酸
△
CH3COOH+C2H5OH CH3COOCH2CH3+H2O
。濃硫酸
△
(2)兩組同學(xué)想要比較所制得的乙酸乙酯的產(chǎn)量,簡便的方法是
使用相同規(guī)格的試管,比較兩支試管中上層液體的高度
使用相同規(guī)格的試管,比較兩支試管中上層液體的高度
。(3)該反應(yīng)為可逆反應(yīng),要提高乙酸乙酯的產(chǎn)率,該實驗中采取的措施有
從反應(yīng)物中不斷的蒸出乙酸乙酯,使用過量的乙酸等都可以使平衡正向移動,從而提高乙酸乙酯的產(chǎn)率
從反應(yīng)物中不斷的蒸出乙酸乙酯,使用過量的乙酸等都可以使平衡正向移動,從而提高乙酸乙酯的產(chǎn)率
。(4)現(xiàn)對全班同學(xué)試管乙中的液體集中處理,得到乙酸乙酯的粗產(chǎn)品并回收乙醇。假設(shè)全班共做10組實驗,得到乙酸乙酯共20.4g,請計算乙酸乙酯的產(chǎn)率為
66.23%
66.23%
(保留兩位有效數(shù)字)。Ⅱ、實驗小組用下列裝置進行實驗。

(1)該實驗的目的是
檢驗乙醇的催化氧化
檢驗乙醇的催化氧化
,請寫出總反應(yīng)化學(xué)方程式 2C2H5OH+O2 2CH3CHO+2H2O
C
u
△
2C2H5OH+O2 2CH3CHO+2H2O
。C
u
△
(2)若想檢驗試管a中收集的液體成分含有乙醛,請分別寫出兩種檢驗方法的主要化學(xué)方程式:
①
CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag+3NH3+H2O
水浴加熱
CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag+3NH3+H2O
;水浴加熱
②
CH3CHO+NaOH+2Cu(OH)2 Cu2O↓+CH3COONa+3H2O
△
CH3CHO+NaOH+2Cu(OH)2 Cu2O↓+CH3COONa+3H2O
。 △
【答案】CH3COOH+C2H5OH CH3COOCH2CH3+H2O;使用相同規(guī)格的試管,比較兩支試管中上層液體的高度;從反應(yīng)物中不斷的蒸出乙酸乙酯,使用過量的乙酸等都可以使平衡正向移動,從而提高乙酸乙酯的產(chǎn)率;66.23%;檢驗乙醇的催化氧化;2C2H5OH+O2 2CH3CHO+2H2O;CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag+3NH3+H2O;CH3CHO+NaOH+2Cu(OH)2 Cu2O↓+CH3COONa+3H2O
濃硫酸
△
C
u
△
水浴加熱
△
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:3引用:1難度:0.5
相似題
-
1.硫鐵礦燒渣是硫鐵礦生產(chǎn)硫酸過程中產(chǎn)生的工業(yè)廢渣(主要含F(xiàn)e2O3及少量SiO2、Al2O3等雜質(zhì)).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如下:
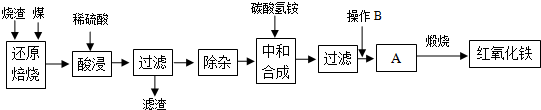
(1)在“還原焙燒”中產(chǎn)生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據(jù)下表數(shù)據(jù):
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應(yīng)小于氫氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,檢驗
Fe3+已經(jīng)除盡的試劑是.
(4)“中和合成”的目的是將溶液中Fe2+轉(zhuǎn)變?yōu)樘妓醽嗚F沉淀,則操作B是.
(5)煅燒A的反應(yīng)方程式是.
(6)a g燒渣經(jīng)過上述工藝可得紅氧化鐵b g.藥典標(biāo)準(zhǔn)規(guī)定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質(zhì)量分?jǐn)?shù)應(yīng)不低于(用含a、b的表達式表示).發(fā)布:2025/1/19 8:0:1組卷:5引用:1難度:0.5 -
2.硫鐵礦燒渣是硫鐵礦生產(chǎn)硫酸過程中產(chǎn)生的工業(yè)廢渣(主要含F(xiàn)e2O3及少量SiO2、Al2O3、CaO、MgO等雜質(zhì)).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如圖:
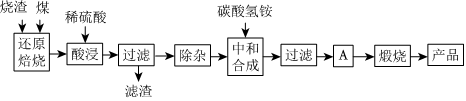
(1)在“還原焙燒”中產(chǎn)生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據(jù)下表數(shù)據(jù):
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應(yīng)小于氫氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,檢驗Fe3+已經(jīng)除盡的試劑是;當(dāng)pH=5時,溶液中c(Al3+)=mol?L-1(已知常溫下Ksp[Al(OH)3]=2.0×10-33).
(4)“中和合成”的目的是將溶液中Fe2+轉(zhuǎn)變?yōu)樘妓醽嗚F沉淀,則A的操作是.
(5)a g燒渣經(jīng)過上述工藝可得紅氧化鐵b g.藥典標(biāo)準(zhǔn)規(guī)定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質(zhì)量分?jǐn)?shù)應(yīng)不低于(用含a、b的表達式表示).發(fā)布:2025/1/19 8:0:1組卷:114引用:4難度:0.5 -
3.硫鐵礦燒渣是硫鐵礦生產(chǎn)硫酸過程中產(chǎn)生的工業(yè)廢渣(主要含F(xiàn)e2O3及少量SiO2、Al2O3、CaO、MgO等雜質(zhì)).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如下:
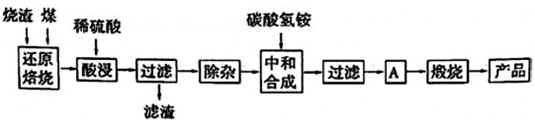
(1)在“還原焙燒”中產(chǎn)生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據(jù)下表數(shù)據(jù):
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應(yīng)小于氫氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,常溫下,當(dāng)pH=5時,溶液中c(Al3+)=mol?L-1(已知常溫下Ksp[Al(OH)3]═2.0×10-33).
(4)“中和合成”的目的是將溶液中Fe2+轉(zhuǎn)變?yōu)樘妓醽嗚F沉淀,則A的操作是.發(fā)布:2025/1/19 8:0:1組卷:12引用:1難度:0.5
相關(guān)試卷


