 碳及其化合物廣泛存在于自然界中,回答下列問題:
碳及其化合物廣泛存在于自然界中,回答下列問題:
(1)處于一定空間運動狀態的電子在原子核外出現的概率密度分布可用電子云電子云形象化描述。在基態14C原子中,核外存在22對自旋相反的電子。
(2)碳在形成化合物時,其鍵型以共價鍵為主,原因是C有4個價電子且半徑較小,難以通過得或失電子達到穩定結構C有4個價電子且半徑較小,難以通過得或失電子達到穩定結構。
(3)CS2分子中,共價鍵的類型有σ鍵和π鍵σ鍵和π鍵,C原子的雜化軌道類型是spsp,寫出兩個與CS2具有相同空間構型和鍵合形式的分子或離子CO2、SCN-或COS等CO2、SCN-或COS等。
(4)CO能與金屬Fe形成Fe(CO)5,該化合物熔點為253K,沸點為376K,其固體屬于分子分子晶體。
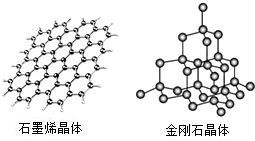
(5)碳有多種同素異形體,其中石墨烯與金剛石的晶體結構如圖所示:
①在石墨烯晶體中,每個C原子連接33個六元環,每個六元環占有22個C原子。
②在金剛石晶體中,C原子所連接的最小環也為六元環,每個C原子連接1212個六元環,六元環中最多有44個C原子在同一平面。
【考點】共價晶體.
【答案】電子云;2;C有4個價電子且半徑較小,難以通過得或失電子達到穩定結構;σ鍵和π鍵;sp;CO2、SCN-或COS等;分子;3;2;12;4
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:1316引用:12難度:0.5
相似題
-
1.下列有關晶體的說法中一定正確的是( )
A.三種晶體的硬度由大到小:金剛石>SiC>晶體硅 B.由于石墨的熔點很高,所以它是共價晶體 C.某晶體中有陽離子一定也有陰離子 D.離子晶體中都含有離子鍵,所以分子晶體中也一定含有共價鍵 發布:2024/12/30 16:0:2組卷:33引用:3難度:0.6 -
2.氮化硅(Si3N4)是一種高溫陶瓷材料,它難溶于水、硬度大、熔點高、化學性質穩定.則由此推測氮化硅是( )
A.離子晶體 B.分子晶體 C.原子晶體 D.金屬晶體 發布:2024/12/30 16:0:2組卷:22引用:3難度:0.9 -
3.下列關于共價晶體、分子晶體的敘述中,正確的是( )
A.在SiO2晶體中,1個硅原子和2個氧原子形成2個共價鍵 B.基態原子的價電子排布為(n-1)dxnsy的元素,族序數一定為x+y C.HCl的相對分子質量大于HF,所以HCl的沸點高于HF D.金剛石為網狀結構,由共價鍵形成的碳原子環中,最小環上有6個碳原子 發布:2024/12/30 15:30:1組卷:49引用:2難度:0.7


