硫酸是世界上產量最大、用途最廣的酸,被稱為“化學工業之母”。科學興趣小組同學對硫酸進行了多角度的研究。
【物理性質】
(1)用溫度計的水銀球一端蘸取濃硫酸,取出后在空氣中放置一段時間,觀察到溫度計示數上升,是因為濃硫酸能吸收 水蒸氣水蒸氣,并放出熱量。
【化學性質】
(2)請利用如圖提供的儀器與藥品,探究稀硫酸與氫氧化鈉溶液的反應。
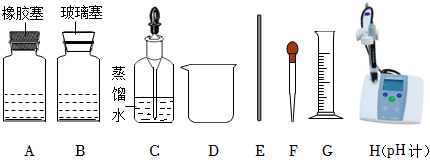
①取 AA (填“A”或“B”)中的氫氧化鈉溶液5mL加入燒杯中,并插入pH計。
②從另一試劑瓶中取出稀硫酸逐滴加入①的溶液中,并用玻璃棒不斷攪拌。反應過程中溶液pH變化的部分數據如表所示:
| 稀硫酸體積/mL | 0 | 2 | 4 | 6 | 8 | …… |
| 溶液pH | 13.1 | 12.8 | 12.3 | 11.5 | 10.4 | …… |
NaOH、Na2SO4
NaOH、Na2SO4
(填化學式)。④滴加稀硫酸過程中,溶液pH不斷減小的原因有:
a.水稀釋氫氧化鈉溶液;
b.
氫氧化鈉和稀硫酸反應,不斷減少
氫氧化鈉和稀硫酸反應,不斷減少
。⑤為證明溶液pH從13.1減小到10.4的過程中,④中原因b起主要作用,需設計的實驗方案是
取等質量的pH=13.1的兩燒杯氫氧化鈉溶液,一杯加入稀硫酸直至pH=10.4,記錄加入稀硫酸的質量。另一杯加入蒸餾水直至pH=10.4,記錄加入蒸餾水的質量,比較加入稀硫酸和蒸餾水的多少
取等質量的pH=13.1的兩燒杯氫氧化鈉溶液,一杯加入稀硫酸直至pH=10.4,記錄加入稀硫酸的質量。另一杯加入蒸餾水直至pH=10.4,記錄加入蒸餾水的質量,比較加入稀硫酸和蒸餾水的多少
。【定量研究】
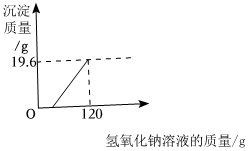
(3)某硫酸工廠排放的廢水中含有硫酸和硫酸銅等有害物質,需要經過處理后才能排放。興趣小組想要測定該廢水中硫酸的含量,取廢水樣品100g,向其中加入溶質質量分數為20%的氫氧化鈉溶液。測得生成的沉淀質量與所加氫氧化鈉溶液的質量關系如圖。根據圖中所得數據計算該硫酸廢水中硫酸的溶質質量分數是多少?(寫出計算過程)
【考點】物質的性質和變化規律的探究.
【答案】水蒸氣;A;NaOH、Na2SO4;氫氧化鈉和稀硫酸反應,不斷減少;取等質量的pH=13.1的兩燒杯氫氧化鈉溶液,一杯加入稀硫酸直至pH=10.4,記錄加入稀硫酸的質量。另一杯加入蒸餾水直至pH=10.4,記錄加入蒸餾水的質量,比較加入稀硫酸和蒸餾水的多少
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:10引用:1難度:0.5
相似題
-
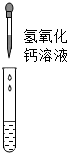 1.小科在課堂活動中進行氫氧化鈣與氯化鐵反應的實驗,實驗操作如圖所示。他發現沒有出現預期的紅褐色沉淀,這是什么原因呢?
1.小科在課堂活動中進行氫氧化鈣與氯化鐵反應的實驗,實驗操作如圖所示。他發現沒有出現預期的紅褐色沉淀,這是什么原因呢?
(1)小科猜想:是不是久置的氫氧化鈣溶液完全變質了?他取少量氫氧化鈣溶液,向其中加入,出現白色沉淀,說明氫氧化鈣沒有完全變質。
(2)小科又想是不是氯化鐵的問題呢?通過查閱資料,小科知道了氯化鐵久置后會轉化成氫氧化鐵。因此實驗室在配制氯化鐵溶液時,總會在溶液中加入少量鹽酸,以防出現氫氧化鐵沉淀。
為了檢驗氯化鐵溶液中是否含有鹽酸,小科設計了以下兩個方案。
方案一:向氯化鐵溶液中加入硝酸銀溶液,觀察是否產生白色沉淀。
方案二:向氯化鐵溶液中加入鎂粉,觀察是否產生氣泡。
小明覺得其中一個方案不可行,請指出該方案并說明理由。
(3)經過實驗驗證,氯化鐵溶液中含有鹽酸。為了得到預期的紅褐色沉淀,若仍用原試劑應如何操作?。發布:2024/12/28 11:30:1組卷:72引用:4難度:0.5 -
2.科學興趣小組探究金屬的性質時,將24克相同表面積的鎂銅合金,均分成兩等份,分別滴加體積相同、溶質質量分數不同的稀鹽酸,在一定條件下反應,測得氣壓變化如圖甲所示。
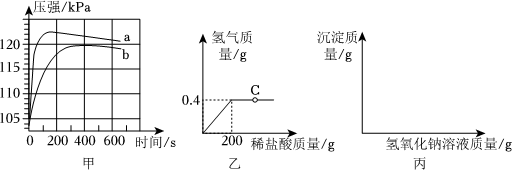
(1)對比圖甲中a、b曲線,引起a曲線壓強增大速度明顯快于b的因素可能是。(列舉一點即可)
(2)其中有一組實驗是滴加7.3%稀鹽酸,產生氫氣的質量隨加入鹽酸的質量變化情況如圖乙所示。
①圖乙中當剛好生成0.4克氫氣時,所得溶液中溶質是(填化學式);鎂銅合金中鎂的質量分數為多少?(寫出計算過程)
②將圖乙中C點對應的溶液過濾,向濾液中逐滴加入過量氫氧化鈉溶液。在圖丙中標出產生氫氧化鎂沉淀質量隨滴加氫氧化鈉質量的大致變化曲線。(圖中不需注明具體相關質量)發布:2024/10/23 0:0:2組卷:12引用:1難度:0.5 -
3.使用如圖所示裝置(攪拌裝置略)探究溶液離子濃度變化,已知反應的產物如果全部是沉淀(或沉淀和水)時燈光會變暗。下列燈光變化可能出現“亮→暗(或滅)→亮”現象的是( )
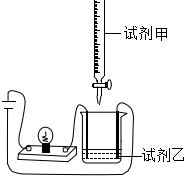
試劑甲 試劑乙 A MgSO4 Ba(OH)2 B K2CO3 HNO3 C HNO3 KOH D NaCl AgNO3 A.A B.B C.C D.D 發布:2024/11/28 6:0:2組卷:37引用:3難度:0.5


