 某興趣小組為驗證質量守恒定律,做了鎂條在空氣中燃燒的實驗。
某興趣小組為驗證質量守恒定律,做了鎂條在空氣中燃燒的實驗。
(1)請寫出鎂條與氧氣反應的化學方程式:2Mg+O2 點燃 2MgO2Mg+O2 點燃 2MgO。
(2)小明發現燃燒產物的質量大于反應物鎂條的質量,認為這個反應不遵守質量守恒定律,我 不同意不同意(“同意”或“不同意”)小明的觀點,因為 任何化學反應都遵循質量守恒定律,該反應前后質量不相等的原因是空氣中有氣體參與了反應任何化學反應都遵循質量守恒定律,該反應前后質量不相等的原因是空氣中有氣體參與了反應。
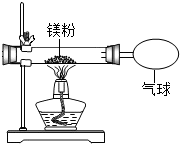
(3)小紅按如圖裝置改進實驗,驗證了質量守恒定律,卻發現產物中還有少量黃色固體。
【提出問題】黃色固體是什么呢?
【查閱資料】
①氧化鎂為白色固體;
②鎂能與氮氣反應生成黃色的氮化鎂(Mg3N2)固體;
③氮化鎂可與水劇烈反應產生氨氣,該氣體能使濕潤的紅色石蕊試紙變藍。
【做出猜想】黃色固體為Mg3N2
【實驗探究】請設計實驗,驗證猜想
點燃
點燃
| 實驗操作 | 實驗現象及結論 |
|
取燃燒后的產物于試管中,加少量水,再將濕潤的紅色石蕊試紙放在試管口,觀察現象 取燃燒后的產物于試管中,加少量水,再將濕潤的紅色石蕊試紙放在試管口,觀察現象
|
若產生使濕潤的紅色石蕊試紙變藍的氣體, 說明燃燒產物中含有Mg3N2 若產生使濕潤的紅色石蕊試紙變藍的氣體,
說明燃燒產物中含有Mg3N2 |
氧氣比氮氣的化學性質更活潑
氧氣比氮氣的化學性質更活潑
。(4)①若用鎂來代替紅磷測定空氣中氧氣的含量,實驗所測得氧氣的體積分數
大于
大于
(填“大于”“小于”“等于”)1
5
②將7.2g鎂條放在某一足量混合氣體(只有氮氣和氧氣)中燃燒,充分反應后,生成的固體物質的質量取值范圍是:
10g~12g
10g~12g
。【考點】質量守恒定律的實驗探究.
【答案】2Mg+O2 2MgO;不同意;任何化學反應都遵循質量守恒定律,該反應前后質量不相等的原因是空氣中有氣體參與了反應;取燃燒后的產物于試管中,加少量水,再將濕潤的紅色石蕊試紙放在試管口,觀察現象;若產生使濕潤的紅色石蕊試紙變藍的氣體,
說明燃燒產物中含有Mg3N2;氧氣比氮氣的化學性質更活潑;大于;10g~12g
點燃
說明燃燒產物中含有Mg3N2;氧氣比氮氣的化學性質更活潑;大于;10g~12g
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:40引用:4難度:0.6
相似題
-
1.某學生為了探究甲烷的組成元素,設計并完成了如下探究實驗,請你幫他完成下面的實驗報告:
提出問題:甲烷中含有哪些元素?
【查閱資料】含碳元素的物質完全燃燒生成CO2。
實驗探究:
(4)表達與交流:實驗步驟 實驗現象 解釋與結論 ①在空氣中點燃甲烷,
②將潔凈干燥的小燒杯罩在甲烷燃燒的火焰上方。燒杯內壁有水珠。 (1)證明生成物有水,甲烷中一定含有 元素。③將蘸有澄清石灰水的小燒杯罩在甲烷燃燒的火焰上方。 (2) 。(3)證明生成物有CO2.甲烷中一定含有 元素。
經實驗測定甲烷的化學式為CH4,請你寫出甲烷燃燒方程式:。發布:2024/12/1 8:0:1組卷:6引用:1難度:0.5 -
2.某地農民將玉米秸稈等粉碎后放在密閉的沼氣池內發酵制沼氣,發酵后的殘余物可做農家肥。我校化學興趣小組的同學圍繞“玉米秸稈主要由哪些元素組成”的問題展開了以下探究活動:
【猜想與假設】:根據沼氣的成分猜想玉米秸稈中主要含有碳元素和氫元素。
【設計方案】:
【實驗分析】:探究步驟 預計現象 相關結論 用坩堝鉗夾持一小段烘干的玉米秸稈,點燃后伸入盛有氧氣的集氣瓶中 玉米秸稈劇烈燃燒,火焰熄滅后能夠觀察到瓶壁上有水珠 產物中有 向集氣瓶中滴入少量 能夠觀察到 產物中有CO2
(1)將玉米秸稈烘干的目的是:。
(2)根據以上探究,同學們得出結論,秸稈中一定含有元素,可能含有元素(填元素符號)。發布:2024/11/19 8:0:1組卷:8引用:2難度:0.5 -
3.根據以下實驗方案,“探究參加化學反應前后各物質的質量總和是否相等”,請將你的思考及實驗結果寫在短線處。
【猜想假設】:
(1)猜想1:相等;猜想2:。
【實驗探究】
(2)
【反思評價】實驗方案 方案一 方案二 實驗裝置 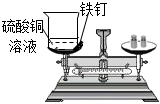
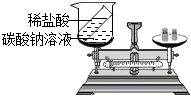
實驗過程 分別將反應物及反應容器放在托盤天平上用砝碼平衡 取下燒杯,將鐵釘浸到硫酸銅溶液中,觀察到的現象是 、溶液由藍色逐漸變為淺綠色;再將其放回托盤天平,天平的指針(填“向左”或“向右”或“不”)偏轉。取下燒杯并將其傾斜,使小試管中的鹽酸進入燒杯中,充分反應后再放回托盤天平,天平的指針 (填“向左”或“向右”或“不”)偏轉,其原因是。
(3)你認為猜想是錯誤的,能用來驗證質量守恒定律的反應需要滿足的條件是。發布:2024/12/25 10:18:46組卷:12引用:2難度:0.5


