當前位置:
試題詳情
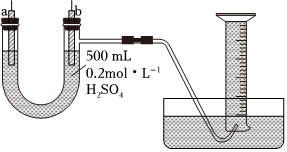 Ⅰ.現用如圖裝置來測定某原電池工作時在某段時間內通過導線的電子的物質的量。量筒的規格為1000mL,供選擇的電極材料有純銅片和純鋅片。請回答下列問題:
Ⅰ.現用如圖裝置來測定某原電池工作時在某段時間內通過導線的電子的物質的量。量筒的規格為1000mL,供選擇的電極材料有純銅片和純鋅片。請回答下列問題:
(1)b電極材料為 純銅片純銅片,其電極反應式為 2H++2e-═H2↑2H++2e-═H2↑。
(2)當量筒中收集到672mL(標準狀況下)氣體時,通過導線的電子的物質的量為 0.06mol0.06mol,此時a電極質量減少 1.951.95g。
Ⅱ.某同學在用稀硫酸與鋅制取氫氣的實驗中,發現加入少量硫酸銅溶液可加快氫氣的生成速率。請回答下列問題:
(1)上述實驗中發生反應的離子方程式有:Zn+2H+═Zn2++H2↑、Zn+Cu2+═Zn2++CuZn+2H+═Zn2++H2↑、Zn+Cu2+═Zn2++Cu。
(2)硫酸銅溶液可以加快氫氣生成速率的原因是 CuSO4與Zn反應產生的Cu與Zn以及硫酸溶液形成Cu/Zn原電池,加快了氫氣產生的速率CuSO4與Zn反應產生的Cu與Zn以及硫酸溶液形成Cu/Zn原電池,加快了氫氣產生的速率。
(3)要加快上述實驗中氣體產生的速率,還可采取的措施有 升高反應溫度升高反應溫度、適當增加硫酸的濃度或增大鋅粒的比表面積適當增加硫酸的濃度或增大鋅粒的比表面積。(答兩種)
(4)為了進一步研究硫酸銅的用量對氫氣生成速率的影響,該同學設計了如下一系列實驗。將表中所給的混合溶液分別加入到6個盛有過量Zn粒的反應瓶中,收集產生的氣體,記錄獲得相同體積的氣體所需時間。(假設混合溶液總體積等于混合前各溶液的體積之和)
| 實驗 混合溶液 |
A | B | C | D | E | F |
| 4mol/L H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 飽和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O /mL | V7 | V8 | V9 | V10 | 10 | 0 |
30
30
,V8=19.5
19.5
。②該同學最后得出的結論為:當加入少量CuSO4溶液時,生成氫氣的速率會大大提高。但當加入的CuSO4溶液超過一定量時,生成氫氣的速率反而會下降。請分析氫氣生成速率下降的主要原因
當加入一定量的CuSO4后,生成的Cu會沉積在Zn的表面,降低了Zn與溶液的接觸面積,使得生成氫氣的速率下降
當加入一定量的CuSO4后,生成的Cu會沉積在Zn的表面,降低了Zn與溶液的接觸面積,使得生成氫氣的速率下降
。③實驗A測得:收集到產生H2體積為112mL(標準狀況下)時所需的時間為10分鐘,求化學反應速率ν(H2SO4)=
0.01mol/(L?min)
0.01mol/(L?min)
。(忽略反應前后溶液體積變化)【考點】探究影響化學反應速率的因素;原電池與電解池的綜合.
【答案】純銅片;2H++2e-═H2↑;0.06mol;1.95;Zn+2H+═Zn2++H2↑、Zn+Cu2+═Zn2++Cu;CuSO4與Zn反應產生的Cu與Zn以及硫酸溶液形成Cu/Zn原電池,加快了氫氣產生的速率;升高反應溫度;適當增加硫酸的濃度或增大鋅粒的比表面積;30;19.5;當加入一定量的CuSO4后,生成的Cu會沉積在Zn的表面,降低了Zn與溶液的接觸面積,使得生成氫氣的速率下降;0.01mol/(L?min)
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:28引用:2難度:0.3
相似題
-
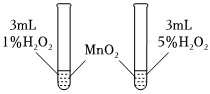 1.控制變量法是化學實驗的常用方法之一,如圖所示實驗探究影響反應速率的因素是( )
1.控制變量法是化學實驗的常用方法之一,如圖所示實驗探究影響反應速率的因素是( )A.催化劑 B.溫度 C.濃度 D.壓強 發布:2024/12/30 14:0:1組卷:44引用:3難度:0.6 -
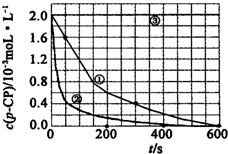 2.(一)Fenton法常用于處理含有難降解有機物的工業廢水,通常是在調節好pH和Fe2+濃度的廢水中加入H2O2,所產生的羥基自由基能氧化降解污染物.現運用該方法降解有機污染物p-CP,探究有關因素對該降解反應速率的影響.實驗中控制p-CP的初始濃度相同,恒定實驗溫度在298K或313K下設計如下對比實驗(其余實驗條件見下表):
2.(一)Fenton法常用于處理含有難降解有機物的工業廢水,通常是在調節好pH和Fe2+濃度的廢水中加入H2O2,所產生的羥基自由基能氧化降解污染物.現運用該方法降解有機污染物p-CP,探究有關因素對該降解反應速率的影響.實驗中控制p-CP的初始濃度相同,恒定實驗溫度在298K或313K下設計如下對比實驗(其余實驗條件見下表):
(1)編號③的實驗目的是實驗序號 實驗目的 T/K pH c/10-3mol?L-1 H2O2 Fe2+ ① 為以下實驗作參照物 298 3 6.0 0.30 ② 探究溫度對降解反應速率的影響 313 3 6.0 0.30 ③ 298 10 6.0 0.30 .
(2)實驗測得不同實驗編號中p-CP的濃度隨時間變化的關系如圖所示.請根據實驗①曲線,計算降解反應在50-300s內的平均反應速率v(p-CP)=.
(3)實驗①②表明,溫度與該降解反應速率的關系是.
(二)已知Fe3+和I-在水溶液中的反應為2I-+2Fe3+=2Fe2++I2.正向反應速率和I-、Fe3+的濃度關系為v=kcm(I-)cn(Fe3+)(k為常數)
(4)請分析下表提供的數據回答以下問題:
①在v=kcm(I-)cn(Fe3+)中,m、n的值為c(I-)/(mol?L-1) c(Fe3+)/(mol?L-1) v/(mol?L-1?s-1) (1) 0.20 0.80 0.032k (2) 0.60 0.40 0.144k (3) 0.80 0.20 0.128k .(選填A、B、C、D)
A.m=1,n=1 B.m=1,n=2 C.m=2,n=1 D.m=2,n=2
②I-濃度對反應速率的影響Fe3+濃度對反應速率的影響(填“<”、“>”或“=”).
(三)一定溫度下,反應FeO(s)+CO(g)?Fe(s)+CO2(g)的化學平衡常數為3.0,該溫度下將2mol FeO、4mol CO、5mol Fe、6mol CO2加入容積為2L的密閉容器中反應.請通過計算回答:
(5)v(正)v(逆)(填“>”、“<”或“=”);若將5mol FeO、4mol CO加入同樣的容器中,在相同溫度下達到平衡,則CO的平衡轉化率為.發布:2024/12/30 14:30:1組卷:19引用:2難度:0.5 -
3.為探究影響化學反應速率的因素,某研究小組設計了如下五個實驗。按要求回答下列問題(已知:Cu2+、Fe3+對H2O2的分解起催化作用)。
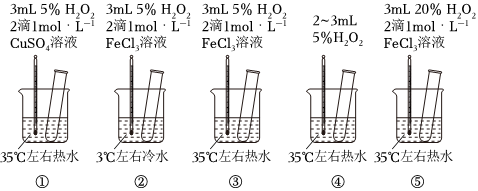
(1)為探究溫度對化學反應速率的影響,應選擇實驗(填序號,下同),選擇的依據是。
(2)為探究催化劑對化學反應速率的影響,同時探究催化劑不同催化效果不同,應選擇實驗。
(3)通過觀察發現實驗⑤比實驗③現象明顯,其原因是。
(4)根據上述實驗,用H2O2快速制取少量O2,可采取的三條措施為。發布:2024/12/30 14:30:1組卷:8引用:5難度:0.5


