當前位置:
試題詳情
 X、Y、Z、L四種元素分別位于周期表中三個緊相鄰的周期且原子序數依次增大,它們相關信息如下:
X、Y、Z、L四種元素分別位于周期表中三個緊相鄰的周期且原子序數依次增大,它們相關信息如下:
X元素原子的價電子構型為nSnnP2n
Y 和Z位于同一周期,最外層都有兩個未成對電子
L元素原子的基態未成對電子數是同周期最多的元素
請回答如下問題:
(1)L元素在周期表中的位置是第四周期ⅥB族第四周期ⅥB族,該原子核外電子排布式是1s22s22p63s23p63d54s11s22s22p63s23p63d54s1,其最高正價氧化物對應的水氧化物的化學式是H2CrO4、H2Cr2O7H2CrO4、H2Cr2O7
(2)元素X與Y形成的化合物晶體類型是晶體原子晶體原子晶體,1mol該化合物含有的化學鍵數為4NA4NA(用阿伏加德羅常數NA 表示)
(3)元素M是周期表中電負性最強的元素,X與M形成的化合物XM2的分子幾何構型是V型V型,該化合物中X的原子的雜化軌道類型是sp3sp3
(4)X與碳、氫、三種元素形成的相對分子質量最小的分子里有個33δ鍵,11個π鍵
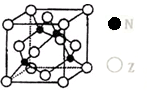
(5)金屬元素N與Z形成的離子化合物的晶胞結構如圖,晶胞中Z離子數目為44。
【答案】第四周期ⅥB族;1s22s22p63s23p63d54s1;H2CrO4、H2Cr2O7;原子晶體;4NA;V型;sp3;3;1;4
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/12/21 8:0:2組卷:73引用:3難度:0.1
相似題
-
1.X、Y、Z、M、N均為短周期主族元素,原子序數依次增大。X是宇宙中含量最高的元素,YX3分子呈三角錐形,Z的價電子排布式為nsnnpn+2,五種元素中M的電負性最小,N的最高價含氧酸酸性最強。下列說法正確的是( )
A. 的VSEPR模型為V形YZ-2B.由X、Y、Z三種元素組成的化合物的水溶液均顯酸性 C.同周期中第一電離能大于Z的元素有3種 D.MN晶體中M離子的配位數為8 發布:2025/1/5 8:0:1組卷:47引用:1難度:0.5 -
2.已知A、B、C、D、E、F、G都是短周期的元素,它們的原子序數依次遞增.A原子的電子層數與它的核外電子總數相同,而B原子的最外層電子數是次外層的2倍,C的氫化物可使濕潤的紅色石蕊試紙變藍,B和D可以形成兩種氣態化合物,E原子核外電子總數比B的2倍少1,D與F同主族,G的原子半徑是本周期元素中最小的.則:
(1)A元素為C元素為E元素為
(2)由上述元素形成的10電子分子有、.
(3)由B和D以質量比為3:8組成的化合物與E的同周期相鄰主族元素的單質反應的化學方程式為.
(4)G單質與E的最高價氧化物的水化物反應的離子方程式為
(5)B、C、D形成的氣態氫化物中,較穩定的是
(6)由A、C、G形成的離子化合物的化學式是.發布:2024/12/30 18:30:1組卷:7引用:3難度:0.5 -
3.A、B、C、D、E為原子序數依次增大的五種短周期元素;A是宇宙中最豐富的元素且與E同主族;B位于元素周期表ⅣA族;C在元素周期表中與B、D相鄰;D基態原子的s軌道與p軌道的電子總數相等且p軌道有2個未成對的電子;E是短周期中原子半徑最大的元素;F原子核外電子數為29.回答下列問題:
(1)F基態原子的核外電子排布式為。
(2)A、B、C、D、E五種元素中,電負性最小的元素為(填元素符號,下同),第一電離能最大的元素為;A3D+的立體構型為。
(3)A、B可形成多種化合物,其中相對分子質量為28的分子,其中心原子的雜化方式為,該分子中σ鍵和π鍵的數目之比為。
(4)化合物BD2和E2D2的晶體類型分別為、。
(5)F單質為面心立方晶體,若F的相對原子質量為M,阿伏加德羅常數為NA,晶胞邊長為a cm,則晶體F的密度ρ=g?cm-3。發布:2025/1/18 8:0:1組卷:27引用:2難度:0.3


