(1)25℃時,電離平衡常數:
| 化學式 | CH3COOH | H2CO3 | HClO |
| 電離平衡常數 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 |
4.0×10-8 |
①當三種酸的物質的量濃度相同時,c(H+)由大到小的順序是
CH3COOH>H2CO3>HClO
CH3COOH>H2CO3>HClO
(用化學式表示,下同)。②同體積、同物質的量濃度的三種酸,中和NaOH的能力(消耗NaOH體積)由大到小的順序是
H2CO3>CH3COOH=HClO
H2CO3>CH3COOH=HClO
。③在一條件下,CH3COOH溶液中存在電離平衡:CH3COOH?CH3COO-+H+△H>0,下列方法中,可以使0.10mol/LCH3COOH溶液中CH3COOH電離程度增大的是
bc
bc
。a.加入少量0.10mol/L的稀鹽酸
b.加熱
c.加水稀釋至0.010mol/L
d.加入少量冰醋酸
e.加入少量氯化鈉固體
④常溫下,0.1mol/L的CH3COOH液加水稀釋過程中,下列表達式的數據一定變小的是
a
a
。a.c(H+)
b.
c
(
H
+
)
c
(
CH
3
COOH
)
c.c(H+)?c(OH-)
d.
c
(
O
H
-
)
c
(
H
+
)
⑤體積為10mLpH=2的醋酸溶液與一元酸HX分別加水稀釋至1000mL,稀釋過程pH變化如圖。溶液稀釋后,HX溶液中水電離出來的c(H+)
大于
大于
醋酸溶液水電離出來c(H+)(填“大于”、“等于”或“小于”)。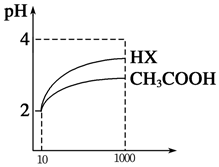
(2)已知純水中存在如下平衡:H2O?H++OH-。現欲使平衡逆向移動,且所得溶液顯酸性,可選擇的方法是
bd
bd
(填字母序號)。a.向水中加入NaOH固體
b.向水中加入NaHSO4固體
c.加熱至100℃
d.向水中通入CO2氣體
(3)常溫下,將pH=11的NaOH溶液與pH=4的硫酸混合,所得溶液的pH=9,則酸、堿溶液的體積比是
9:1
9:1
。【答案】CH3COOH>H2CO3>HClO;H2CO3>CH3COOH=HClO;bc;a;大于;bd;9:1
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:8引用:1難度:0.6
相似題
-
1.25℃時,用蒸餾水稀釋0.10mol?L-1的醋酸,若用KW表示水的離子積常數,則下列各式表 示的數值隨水量的增加而增大的是( )
A. [CH3COOH][H+]B. [CH3COO-][CH3COOH]C. [H+]kWD. [H+][OH-]發布:2025/1/1 8:0:2組卷:1引用:1難度:0.7 -
2.用水稀釋0.1mol/L的醋酸溶液,其中隨加水量的增加而增大的有( )
A.C(CH3COOH) B.C(H+) C.C(H+)/C(CH3COOH) D.C(CH3COOH)/C(H+) 發布:2025/1/1 8:0:2組卷:3引用:1難度:0.9 -
3.將0.1mol?L-1的醋酸溶液加水稀釋,則( )
A.中和此溶液所需的0.1 mol?L-1 NaOH溶液的體積增加 B.c(CH3COOH)減小,平衡向電離方向移動,c(CH3COO-)增大 C.平衡向電離方向移動,c(CH3COOH)、c(H+)、c(OH-)、c(CH3COO-)均減小 D.電離程度增大,由CH3COOH電離出的n(H+)變大 發布:2025/1/1 8:0:2組卷:6引用:1難度:0.7


