硫化氫的轉(zhuǎn)化是資源利用和環(huán)境保護(hù)的重要研究課題。
(1)工業(yè)上將含有硫化物的廢水(以H2S、HS-、S2-的形式存在)引入氧化池,加入高錳酸鉀溶液氧化。已知高錳酸鉀在酸性條件下的還原產(chǎn)物為Mn2+,堿性條件下的為MnO2。
①pH>7時(shí)高錳酸鉀將廢水中的硫化物氧化為S,該反應(yīng)的離子方程式為 2MnO-4+3S2-+4H2O=2MnO2↓+3S↓+8OH-或2MnO-4+3HS-+H2O=2MnO2↓+3S↓+5OH-或2MnO-4+3H2S=2MnO2↓+3S↓+2H2O+2OH-2MnO-4+3S2-+4H2O=2MnO2↓+3S↓+8OH-或2MnO-4+3HS-+H2O=2MnO2↓+3S↓+5OH-或2MnO-4+3H2S=2MnO2↓+3S↓+2H2O+2OH-。
②研究發(fā)現(xiàn):其他條件相同時(shí),廢水呈酸性時(shí)硫化物的去除率明顯大于呈堿性時(shí)去除率,則可能的原因 等物質(zhì)的量的高錳酸鉀在酸性條件下轉(zhuǎn)移的電子數(shù)目比堿性條件下多等物質(zhì)的量的高錳酸鉀在酸性條件下轉(zhuǎn)移的電子數(shù)目比堿性條件下多。
(2)常溫下,H2S的Ka1=1.3×10-7、Ka2=7.0×10-15,Ksp(MnS)=1.4×10-15。向含有0.0020mol?L-1Mn2+廢水中通入一定量的H2S,當(dāng)溶液的pH=a、c(HS-)=1.0×10-4mol?L-1時(shí),Mn2+開始沉淀,則a= 66。
(3)表面噴淋水的活性炭可用于吸附氧化H2S,其原理可用圖1表示。其它條件不變時(shí),水膜的酸堿性與厚度會(huì)影響H2S的去除率。
①適當(dāng)增大活性炭表面的水膜pH,H2S的氧化去除率增大的原因是 OH-濃度增大,促進(jìn)H2S?H++HS-平衡向正反應(yīng)方向移動(dòng),HS-濃度增大OH-濃度增大,促進(jìn)H2S?H++HS-平衡向正反應(yīng)方向移動(dòng),HS-濃度增大。
②若水膜過厚,H2S的氧化去除率減小的原因是 若水膜過厚,導(dǎo)致活性炭的吸附力減弱,吸附的硫化氫、氧氣減少,去除率減少若水膜過厚,導(dǎo)致活性炭的吸附力減弱,吸附的硫化氫、氧氣減少,去除率減少。

(4)甲硫醇是一種惡臭、有毒物質(zhì)。生物法去除甲硫醇反應(yīng)為2CH3SH+7O2═2CO2+2H2O+2H2SO4。研究表明,在H2S存在條件下,可改變甲硫醇(用 表示)生物降解途徑,反應(yīng)歷程如圖2所示,請(qǐng)用簡潔的語言描述圖中甲硫醇的降解過程 在H2S存在條件下,H2S被氧化為S8,S8與甲硫醇
表示)生物降解途徑,反應(yīng)歷程如圖2所示,請(qǐng)用簡潔的語言描述圖中甲硫醇的降解過程 在H2S存在條件下,H2S被氧化為S8,S8與甲硫醇 反應(yīng)生成
反應(yīng)生成 和
和 ,最后
,最后 和
和 和氧氣反應(yīng)生成SO2-4在H2S存在條件下,H2S被氧化為S8,S8與甲硫醇
和氧氣反應(yīng)生成SO2-4在H2S存在條件下,H2S被氧化為S8,S8與甲硫醇 反應(yīng)生成
反應(yīng)生成 和
和 ,最后
,最后 和
和 和氧氣反應(yīng)生成SO2-4。
和氧氣反應(yīng)生成SO2-4。
M
n
O
-
4
M
n
O
-
4
M
n
O
-
4
M
n
O
-
4
M
n
O
-
4
M
n
O
-
4
 反應(yīng)生成
反應(yīng)生成 和
和 ,最后
,最后 和
和 和氧氣反應(yīng)生成
和氧氣反應(yīng)生成SO
2
-
4
 反應(yīng)生成
反應(yīng)生成 和
和 ,最后
,最后 和
和 和氧氣反應(yīng)生成
和氧氣反應(yīng)生成SO
2
-
4
【考點(diǎn)】硫化氫.
【答案】2+3S2-+4H2O=2MnO2↓+3S↓+8OH-或2+3HS-+H2O=2MnO2↓+3S↓+5OH-或2+3H2S=2MnO2↓+3S↓+2H2O+2OH-;等物質(zhì)的量的高錳酸鉀在酸性條件下轉(zhuǎn)移的電子數(shù)目比堿性條件下多;6;OH-濃度增大,促進(jìn)H2S?H++HS-平衡向正反應(yīng)方向移動(dòng),HS-濃度增大;若水膜過厚,導(dǎo)致活性炭的吸附力減弱,吸附的硫化氫、氧氣減少,去除率減少;在H2S存在條件下,H2S被氧化為S8,S8與甲硫醇 反應(yīng)生成
反應(yīng)生成 和
和 ,最后
,最后 和
和 和氧氣反應(yīng)生成
和氧氣反應(yīng)生成
M
n
O
-
4
M
n
O
-
4
M
n
O
-
4
 反應(yīng)生成
反應(yīng)生成 和
和 ,最后
,最后 和
和 和氧氣反應(yīng)生成
和氧氣反應(yīng)生成SO
2
-
4
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:46引用:2難度:0.7
相似題
-
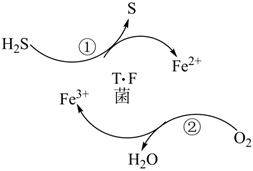 1.天然氣中含有少量H2S等氣體、在酸性溶液中T.f菌可實(shí)現(xiàn)催化脫硫,其原理如圖所示。下列說法錯(cuò)誤的是( )
1.天然氣中含有少量H2S等氣體、在酸性溶液中T.f菌可實(shí)現(xiàn)催化脫硫,其原理如圖所示。下列說法錯(cuò)誤的是( )A.①②均為氧化還原反應(yīng) B.每處理1分子H2S,轉(zhuǎn)移1個(gè)電子 C.反應(yīng)前后Fe3+濃度基本保持不變 D.①反應(yīng)中H2S被氧化 發(fā)布:2024/7/1 8:0:9組卷:24引用:0難度:0.7 -
2.將H2S和空氣的混合氣體通入FeCl2、CuCl2、FeCl3的混合溶液中反應(yīng)回收S,其物質(zhì)轉(zhuǎn)化如圖所示。下列說法正確的是( )

A.在圖示轉(zhuǎn)化中,化合價(jià)不變的元素只有銅、氫 B.過程Ⅲ反應(yīng)的離子方程式為2Fe3++S2-=2Fe2++S↓ C.通入過量的氧氣或者增大Fe3+的濃度可以減少回收的S中CuS的含量 D.有1molH2S轉(zhuǎn)化為硫單質(zhì)時(shí),理論上消耗O2的物質(zhì)的量為2mol[若溶液中n(Fe3+)不變] 發(fā)布:2024/11/14 5:0:2組卷:105引用:2難度:0.7 -
3.H2S是一種高毒性、高腐蝕性的氣體污染物.最新研究表明,在多孔炭材料上搭載活性組分催化氧化脫硫效果明顯優(yōu)于傳統(tǒng)的吸附法,其反應(yīng)機(jī)理如圖所示,此時(shí)H2S在水中濃度為0.34g/100mL。下列有關(guān)說法不正確的是( )
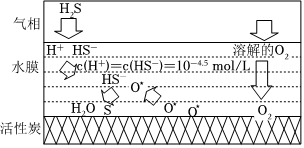
A.活性炭的作用為吸附劑和降低反應(yīng)的活化能 B.H2S的一級(jí)電離常數(shù)為10-9 C.該反應(yīng)的總反應(yīng)方程式為:2H2S+O2=2S+2H2O D.溫度過高不利于脫硫的效果 發(fā)布:2024/7/24 8:0:9組卷:3引用:1難度:0.8
相關(guān)試卷


