乙酰基二茂鐵常用作火箭燃料添加劑、汽油抗爆劑等。某興趣小組制備乙酰基二茂鐵,流程如圖1:
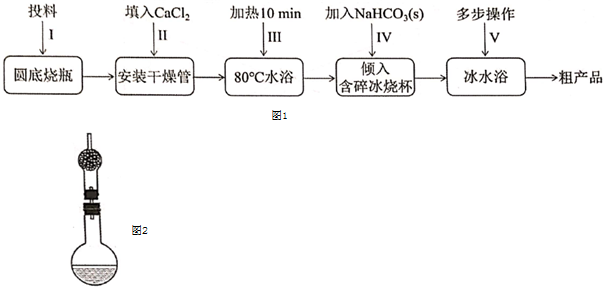
已知:
a.反應原理: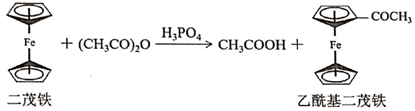
b.二茂鐵熔點173℃,沸點249℃,100℃易升華。
c.乙酰基二茂鐵熔點81℃,沸點163℃.不溶于水,易溶于有機溶劑。
請回答
(1)步驟Ⅰ,在50mL圓底燒瓶中,加入新制的、經提純后0.5g二茂鐵,5mL乙酸酐,在振搖下滴入1mL 85%磷酸,提純二茂鐵的方法為升華升華。
(2)步驟Ⅱ,加料畢,用裝填有CaCl2的干燥管塞住圓底燒瓶瓶口。如圖2所示,其目的是防止空氣中水進入燒瓶,使乙酸酐水解防止空氣中水進入燒瓶,使乙酸酐水解。
(3)步驟Ⅳ,反應完畢后,將紫色混合物傾入含40g碎冰燒杯中,并用10mL冷水洗滌燒瓶,將洗滌液并入燒杯,在攪拌下加入NaHCO3(s),判斷溶液呈中性的實驗方法為加碳酸氫鈉固體至溶液中不再產生氣泡或用pH計檢測溶液pH值加碳酸氫鈉固體至溶液中不再產生氣泡或用pH計檢測溶液pH值。
(4)步驟V,包括結晶、吸濾、洗滌、干燥等多步操作。下列說法正確的是ABAB。
A.為較快地析出晶體,可以用玻璃棒摩擦燒杯內壁
B.吸濾裝置由吸濾瓶、布氏漏斗、抽氣泵組成
C.宜用乙醇洗滌,洗滌后乙醇易揮發
D.可在100℃紅外燈下干燥
(5)①粗產品中含有雜質為二茂鐵或二乙酰基二茂鐵二茂鐵或二乙酰基二茂鐵,可以用來鑒別的儀器是核磁共振、紅外光譜核磁共振、紅外光譜。
②分離提純粗產品后,用薄層層析來測定Rf值。選出其正確操作并按序列出字母
a→c→(bb)→(ff)→(dd)→(ee)→g
a.制備薄層色譜板
b.用少量純二茂鐵和提純后的產品分別溶于2mL甲苯中,配成濃溶液
c.用細玻璃管拉制兩根微量滴管(尖端處約0.7mm)
d.將色譜板插入盛有乙醚的槽內,蓋上蓋子
e.待溶劑上升到色譜板34高度時,取出色譜板,并標記溶劑所到高度
f.分別用微量滴管浸入兩濃溶液,在色譜板兩原點處點樣,待干燥后,再重復點樣
g.計算Rf值
3
4
【考點】制備實驗方案的設計.
【答案】升華;防止空氣中水進入燒瓶,使乙酸酐水解;加碳酸氫鈉固體至溶液中不再產生氣泡或用pH計檢測溶液pH值;AB;二茂鐵或二乙酰基二茂鐵;核磁共振、紅外光譜;b;f;d;e
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:30引用:2難度:0.5
相似題
-
1.硫鐵礦燒渣是硫鐵礦生產硫酸過程中產生的工業廢渣(主要含Fe2O3及少量SiO2、Al2O3等雜質).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如下:
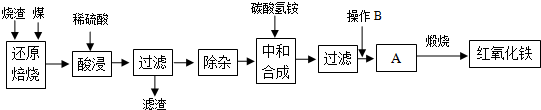
(1)在“還原焙燒”中產生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據下表數據:
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,檢驗
Fe3+已經除盡的試劑是.
(4)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則操作B是.
(5)煅燒A的反應方程式是.
(6)a g燒渣經過上述工藝可得紅氧化鐵b g.藥典標準規定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質量分數應不低于(用含a、b的表達式表示).發布:2025/1/19 8:0:1組卷:5引用:1難度:0.5 -
2.硫鐵礦燒渣是硫鐵礦生產硫酸過程中產生的工業廢渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等雜質).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如圖:
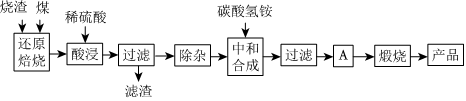
(1)在“還原焙燒”中產生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據下表數據:
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,檢驗Fe3+已經除盡的試劑是;當pH=5時,溶液中c(Al3+)=mol?L-1(已知常溫下Ksp[Al(OH)3]=2.0×10-33).
(4)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則A的操作是.
(5)a g燒渣經過上述工藝可得紅氧化鐵b g.藥典標準規定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質量分數應不低于(用含a、b的表達式表示).發布:2025/1/19 8:0:1組卷:114引用:4難度:0.5 -
3.硫鐵礦燒渣是硫鐵礦生產硫酸過程中產生的工業廢渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等雜質).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如下:
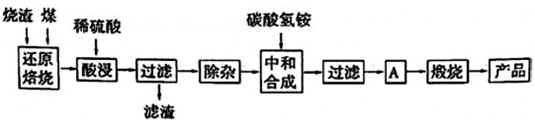
(1)在“還原焙燒”中產生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據下表數據:
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,常溫下,當pH=5時,溶液中c(Al3+)=mol?L-1(已知常溫下Ksp[Al(OH)3]═2.0×10-33).
(4)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則A的操作是.發布:2025/1/19 8:0:1組卷:12引用:1難度:0.5


