當(dāng)前位置:
試題詳情
20世紀(jì)50年代科學(xué)家提出價(jià)層電子對(duì)互斥模型(簡(jiǎn)稱VSEPR模型),用于預(yù)測(cè)簡(jiǎn)單分子立體結(jié)構(gòu)。其要點(diǎn)可以概括為:
Ⅰ.用AXnEm表示只含一個(gè)中心原子的分子組成,A為中心原子,X為與中心原子相結(jié)合的原子,E為中心原子最外層未參與成鍵的電子對(duì)(稱為孤對(duì)電子),(n+m)稱為價(jià)層電子對(duì)數(shù)。分子中的價(jià)層電子對(duì)總是互相排斥,均勻的分布在中心原子周圍的空間;
Ⅱ.分子的立體構(gòu)型是指分子中的原子在空間的排布,不包括中心原子未成鍵的孤對(duì)電子;
Ⅲ.分子中價(jià)層電子對(duì)之間的斥力主要順序?yàn)椋篿、孤對(duì)電子之間的斥力>孤對(duì)電子對(duì)與共用電子對(duì)之間的斥力>共用電子對(duì)之間的斥力;ii、雙鍵與雙鍵之間的斥力>雙鍵與單鍵之間的斥力>單鍵與單鍵之間的斥力;iii、X原子得電子能力越弱,A-X形成的共用電子對(duì)之間的斥力越強(qiáng);iv、其他。
請(qǐng)仔細(xì)閱讀上述材料,回答下列問(wèn)題:
(1)NH4+與CO32-的空間構(gòu)型:NH4+正四面體型正四面體型;CO32-平面正三角形平面正三角形。
(2)有兩種活性反應(yīng)中間體微粒,它們的微粒中均含有1個(gè)碳原子和3個(gè)氨原子。請(qǐng)依據(jù)下面給出的這兩種微粒的球棍模型,寫出相應(yīng)的化學(xué)式:
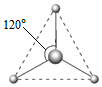 CH3+CH3+;
CH3+CH3+;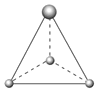 CH3-CH3-。
CH3-CH3-。
(3)按要求寫出第二周期非金屬元素構(gòu)成的中性分子的化學(xué)式:
平面三角形分子 BF3BF3,三角錐形分子 NF3NF3,四面體形分子 CF4CF4。
(4)硼酸晶體構(gòu)型為平面層狀結(jié)構(gòu)(如圖Ⅰ)。四硼酸根為立體結(jié)構(gòu)(如圖Ⅱ)。
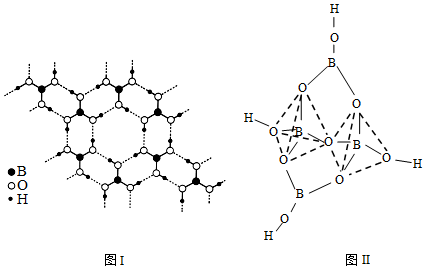
①硼酸為 分子分子晶體:晶體中各層之間的作用力為 范德華力范德華力。
②四硼酸根中硼原子的雜化方式為 sp3sp3。
③與B、O同周期,第一電離能介于二者之間的有 Be、CBe、C(填元素符號(hào))。
【考點(diǎn)】判斷簡(jiǎn)單分子或離子的構(gòu)型.
【答案】正四面體型;平面正三角形;CH3+;CH3-;BF3;NF3;CF4;分子;范德華力;sp3;Be、C
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書(shū)面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:24引用:2難度:0.4
相似題
-
1.根據(jù)VSEPR模型和雜化軌道理論對(duì)磷酸根(
)的空間結(jié)構(gòu)的預(yù)測(cè)和解釋中,完全正確的是( )PO3-4A.磷酸根離子的空間結(jié)構(gòu)為三角錐形 B.中心原子P的價(jià)層電子對(duì)數(shù)為4 C.中心原子P的雜化軌道類型為sp3 D.中心原子P的孤電子對(duì)數(shù)為1 發(fā)布:2025/1/5 8:0:1組卷:6引用:1難度:0.8 -
2.根據(jù)雜化軌道理論和價(jià)層電子對(duì)互斥模型判斷,下列說(shuō)法不正確的是( )
選項(xiàng) 粒子 中心原子雜化方式 VSEPR模型 空間結(jié)構(gòu) A CO2 sp 直線形 直線形 B NH3 sp3 四面體形 三角錐形 C CO2-3sp2 四面體形 平面三角形 D H3O+ sp3 四面體形 三角錐形 A.A B.B C.C D.D 發(fā)布:2025/1/5 8:0:1組卷:78引用:3難度:0.6 -
3.通常把原子總數(shù)和價(jià)電子總數(shù)相同的分子或離子稱為等電子體。人們發(fā)現(xiàn)等電子體的空間結(jié)構(gòu)相同,則下列有關(guān)說(shuō)法中正確的是( )
A.CH4和NH4+是等電子體,鍵角均為60° B.H3O+和PCl3是等電子體,均為平面三角形結(jié)構(gòu) C.NO3-和CO32-是等電子體,均為三角錐形結(jié)構(gòu) D.B3N3H6和苯是等電子體,B3N3H6分子中存在“肩并肩”式重疊的軌道 發(fā)布:2024/12/30 18:0:1組卷:12引用:2難度:0.8


