通過化學學習,我們了解了化學的研究對象是物質,其中研究物質的組成是非常重要的內容之一。圖1是研究物質組成的幾個實驗,請回答下列問題:
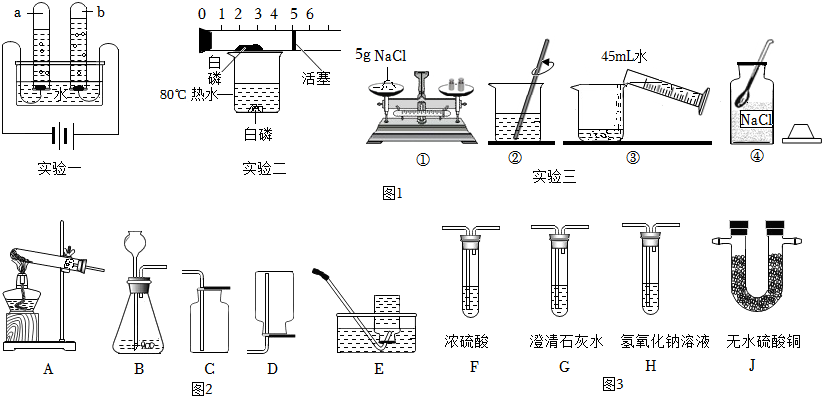
Ⅰ.測定純凈物的組成
實驗一是電解水實驗。
(1)a管中產生的氣體是 氫氣氫氣。
(2)若b試管中產生2mL氣體,則a試管中產生氣體約為 44mL。
(3)a、b試管中氣體物質的質量比為 1:81:8。
(4)該實驗得出水是由 氫元素和氧元素氫元素和氧元素組成的結論,得出該結論的理論依據是 化學反應前后元素種類不變化學反應前后元素種類不變。
Ⅱ.測定混合物的組成。
實驗二是測定空氣中氧氣含量的實驗(已知裝置氣性好,活塞可自由移動)。
(5)白磷燃燒過程中觀察到的實驗現象是:白磷燃燒,產生大量白煙,放熱,活塞先向 右右移動,最終停在刻度4的位置,根據此現象得出的實驗結論是 氧氣在空氣中的體積分數約為15氧氣在空氣中的體積分數約為15。
(6)若白磷量不足,活塞將停在 >>(選填“>”“=”或“<”)4的位置。
(7)該實驗還能同時得出燃燒條件需要氧氣,相應現象是 開始時,帶活塞的管子中白磷燃燒,而燒杯中白磷不燃燒開始時,帶活塞的管子中白磷燃燒,而燒杯中白磷不燃燒。
Ⅲ.測定溶液的定量組成
實驗三是配制一定溶質質量分數的NaCl溶液。
(8)配制該溶液的順序為 ④①③②④①③②(填序號),所得溶液的溶質質量分數是 10%10%(水的密度是1g/mL)。
(9)稱量NaCl固體的過程中,發現托盤天平的指針向左偏轉,此時應該 減少藥品減少藥品(填實驗操作)。
(10)能造成所配溶液溶質質量分數偏小的因素 稱量的NaCl固體中有雜質稱量的NaCl固體中有雜質(寫出一條即可)。
Ⅳ.測定化學反應涉及的相關物質組成
工業焊接、切割金屬經常會用到乙炔氣體,圖2是實驗室可用于制取氧氣和乙炔氣體的裝置。
【查閱材料】
①乙炔(C2H2)是一種無色無味氣體,極難溶于水,密度比空氣略小,乙炔在純氧中燃燒火焰溫度可達3000℃以上,實驗室里常用固體電石(CaC2)與水接觸反應來制取。
②白色無水硫酸銅粉末遇水變成藍色。
【實驗探究】
(11)實驗室用高錳酸鉀取氧氣,應選用的發生裝置是 AA(填序號,下同);制取乙炔氣體,選用的發生裝置 不可以不可以(填“可以”或“不可以”)和高錳酸鉀制氧氣相同,若收集一瓶較純凈的乙炔氣體,選擇的收集裝置是 EE。
(12)探究實驗室制取乙炔氣體后,將剩余物質過濾,所得濾液中溶質的組成,操作過程及結果如下表:
1
5
1
5
| 實驗操作 | 實驗現象 | 實驗結論 |
| ①取少量濾液于試管中,滴加少量酚酞溶液 | 溶液變紅色 | 濾液中的溶質是 氫氧化鈣 氫氧化鈣 。 |
| ②另取少量濾液于試管中,加入碳酸鈉溶液 | 白色沉淀 |
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
。(13)組裝一套測定乙炔氣體完全燃燒后產物組成的實驗,請從圖3中選擇裝置外并按正確順序連接:
JG
JG
(填序號),從而確定乙炔燃燒產物有水和二氧化碳,確定有二氧化碳生成的現象是 澄清石灰水變渾濁
澄清石灰水變渾濁
。【答案】氫氣;4;1:8;氫元素和氧元素;化學反應前后元素種類不變;右;氧氣在空氣中的體積分數約為;>;開始時,帶活塞的管子中白磷燃燒,而燒杯中白磷不燃燒;④①③②;10%;減少藥品;稱量的NaCl固體中有雜質;A;不可以;E;氫氧化鈣;Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;JG;澄清石灰水變渾濁
1
5
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:65引用:3難度:0.4
相似題
-
 1.如圖是某同學設計的測定空氣中氧氣含量的實驗裝置,在具支試管(容積大約120mL)中鋪上一層玻璃棉,用于保護反應管,注射器提前連接好,裝入100mL水,實驗時,將橡皮塞取下,取足量的白磷放入具支試管底部的玻璃棉上,塞緊橡皮塞并用拇指壓住,在試管底部稍微加熱,白磷燃燒。回答下列問題:
1.如圖是某同學設計的測定空氣中氧氣含量的實驗裝置,在具支試管(容積大約120mL)中鋪上一層玻璃棉,用于保護反應管,注射器提前連接好,裝入100mL水,實驗時,將橡皮塞取下,取足量的白磷放入具支試管底部的玻璃棉上,塞緊橡皮塞并用拇指壓住,在試管底部稍微加熱,白磷燃燒。回答下列問題:
(1)待反應結束,裝置完全冷卻后,注射器內的水進入具支試管體積約為mL,因此得出結論:,若進水量偏小,可能的原因是。
(2)整個實驗過程中,活塞先向左運動,原因。
(3)集氣瓶中剩下的氣體主要是哪種氣體,其化學符號表示為,該實驗說明這種氣體具有的物理性質是;化學性質是。
(4)你認為該實驗設計的優點是。發布:2024/10/17 5:0:1組卷:11引用:1難度:0.5 -
 2.某小組設計如圖裝置測定空氣中氧氣含量,膠頭滴管中的水滴入生石灰一段時間后,發現試管內的白磷開始燃燒,待白磷熄滅并冷卻后打開彈簧夾。下列有關該實驗說法正確的是( )?
2.某小組設計如圖裝置測定空氣中氧氣含量,膠頭滴管中的水滴入生石灰一段時間后,發現試管內的白磷開始燃燒,待白磷熄滅并冷卻后打開彈簧夾。下列有關該實驗說法正確的是( )?A.白磷能燃燒,說明生石灰與水反應放熱 B.試管內只需加入少量白磷即可 C.試管內的細沙可吸收產生的物質,防止污染空氣 D.冷卻后,注射器內的活塞最終停留在16mL處 發布:2024/10/19 6:0:3組卷:18引用:1難度:0.5 -
3.隨著科技的進步,越來越多的新技術應用于化學實驗,如傳感技術可以使實驗更加直觀準確。請回答以下實驗中有關問題。
【實驗一】研究主題:空氣中氧氣含量的測定。
(1)為使實驗結果更準確,用圖-1裝置測定氧氣含量前必須檢查。
(2)已知:2Cu+O22CuO。圖-2實驗中,實驗過程中反復推拉注射器的活塞,目的是△。與圖-1實驗相比,圖-2實驗的優點是(答一點)。
(3)圖-2裝置的硬質玻璃管中空氣體積為190mL,反應前注射器活塞位于60mL刻度處,反應后冷卻至室溫注射器活塞位于10mL刻度處(實驗前后氣球都是癟的),則該實驗測得空氣中氧氣的體積分數為。若要得到該實驗結果,至少需要銅粉的質量為(寫出計算過程,計算結果保留至0.01g。常溫常壓下,氧氣的密度約為1.4g/L)。
(4)為了幫助同學們理解圖-1實驗的原理,利用傳感器技術實時測定了圖-1實驗過程中裝置內的壓強、溫度和氧氣濃度的變化,實驗結果如圖-3所示。
①其中X曲線表示的是(填“溫度”或“氧氣濃度”)。
②結合X、Y兩條曲線,解釋圖-3中DE段壓強變化的原因是。
【實驗二】研究主題:用濾紙做“燒不壞的手帕”實驗時,適合的酒精溶液的濃度范圍大致是多少?
【已知】①酒精溶液的濃度=×100%;酒精的質量酒精的質量+水的質量
②濾紙的著火點約為130℃;
③無水酒精的密度為0.8g/mL,水的密度為1.0g/mL。
【實驗步驟】按下表配制不同濃度的酒精溶液,用不同濃度的酒精溶液浸泡濾紙,加熱,用溫度傳感器測定酒精燃燒時濾紙的溫度,所得數據繪制成如圖-4所示的曲線。
??(1)寫出該實驗中酒精(C2H6O)完全燃燒生成水和二氧化碳的化學方程式實驗編號 無水酒精體積/mL 水體積/mL 1 10 5 2 10 10 3 10 15 4 10 20 5 10 30 。
(2)實驗①在接近20s時溫度突然上升的主要原因是。
(3)實驗③大約在s時酒精燃盡,火焰熄滅。
【實驗結論】
(4)根據圖-4分析,用濾紙做“燒不壞的手帕”實驗,為確保實驗成功,所用酒精溶液的濃度范圍大致是28.6%≤ω≤(計算結果保留至0.1%)。
【反思提高】
(5)實驗⑤的曲線與其他4個實驗的曲線比較后,你對物質燃燒條件的新認識是。
(6)用實驗②的酒精溶液實驗時,將濾紙緊緊揉成一團,最后濾紙被燒成灰燼,所以用濃度較大的酒精溶液成功完成“燒不壞的手帕”實驗應該。發布:2024/10/19 9:0:1組卷:69引用:1難度:0.5


