實驗室里用乙醇在170℃、濃硫酸催化下制備乙烯,方程式為C2H5OH→CH2=CH2↑+H2O。乙烯再與溴反應制1,2-二溴乙烷。在制備過程中部分乙醇被濃硫酸氧化產生CO2、SO2,進而與Br2反應生成HBr等酸性氣體。
(1)用下列儀器,以上述三種物質為原料制備1,2-二溴乙烷。如果氣體流向為從左到右,正確的連接順序是(短接口或橡皮管均已略去):B經A①插入A中,D接A②;A③接C接FF接E接GG。
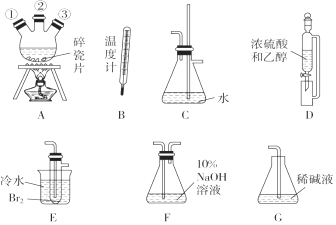
(2)裝置A中碎瓷片的作用是防暴沸防暴沸。若加熱一段時間后,發現碎瓷片忘加,應采取的正確操作是BB。
A.立即補加
B.冷卻后補加
C.不需補加
D.重新配料
(3)裝置C的作用是作安全瓶,防倒吸作安全瓶,防倒吸。
(4)裝置F中盛有10% NaOH溶液的作用是除CO2、SO2等酸性氣體除CO2、SO2等酸性氣體。
(5)在反應管E中進行的主要反應的化學方程式為CH2=CH2+Br2→BrCH2CH2BrCH2=CH2+Br2→BrCH2CH2Br。
【考點】乙醇的消去反應.
【答案】F;G;防暴沸;B;作安全瓶,防倒吸;除CO2、SO2等酸性氣體;CH2=CH2+Br2→BrCH2CH2Br
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:79引用:1難度:0.5
相似題
-
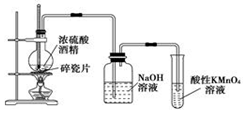 1.實驗室用無水酒精和濃硫酸(體積比1:3)的混合加熱制乙烯氣體。某學習小組設計了如圖所示裝置,用于制取乙烯并驗證乙烯的性質。
1.實驗室用無水酒精和濃硫酸(體積比1:3)的混合加熱制乙烯氣體。某學習小組設計了如圖所示裝置,用于制取乙烯并驗證乙烯的性質。
(1)觀察實驗裝置,判斷本實驗需要驗證乙烯的性質是。
(2)寫出生成乙烯的化學方程式。
(3)混合無水酒精和濃硫酸的具體操作方法是。
(4)在進行以下實驗時,不需要使用溫度計的是(填序號)。
A.制取溴苯 B.制取硝基苯C.蒸餾乙醇和水的混合物 D.制取乙酸乙酯
(5)加熱一段時間后,燒瓶中混合物顏色發黑。則NaOH溶液的作用是。
(6)有同學提出,如果利用溴水替代NaOH和酸性高錳酸鉀溶液,可以驗證乙烯是不飽和烴,利用化學方程式說明該方案的不合理性。發布:2024/12/21 8:0:2組卷:140引用:1難度:0.3 -
2.如圖為實驗室制取乙烯并驗證其性質的裝置圖。下列說法不正確的是( )
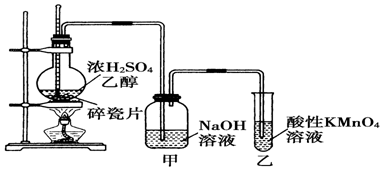
A.反應裝置中濃硫酸和乙醇的體積比約為1:3 B.甲中NaOH溶液的作用是為了除去乙烯中的雜質氣體 C.乙中溶液褪色,證明乙烯具有還原性 D.實驗時,溫度應該迅速升高到170℃并穩定在該溫度最好 發布:2024/12/30 13:30:2組卷:148引用:3難度:0.7 -
 3.已知用P2O5作催化劑,加熱乙醇可制備乙烯,反應溫度為80℃~210℃.某研究性小組設計了如下的裝置制備并檢驗產生的乙烯氣體(夾持和加熱儀器略去).
3.已知用P2O5作催化劑,加熱乙醇可制備乙烯,反應溫度為80℃~210℃.某研究性小組設計了如下的裝置制備并檢驗產生的乙烯氣體(夾持和加熱儀器略去).
(1)儀器a的名稱為.
(2)用化學反應方程式表示上述制備乙烯的原理.
(3)已知P2O5是一種酸性干燥劑,吸水放出大量熱,在實驗過程中P2O5與乙醇能發生作用,因反應用量的不同,會生成不同的磷酸酯,它們均為易溶于水的物質,沸點較低.寫出乙醇和磷酸反應生成磷酸二乙酯的化學方程式(磷酸用結構式表示 ).
).
(4)該裝置中還缺一種必備儀器,該儀器為.某同學認為即使添加了該儀器上述裝置驗證產生了乙烯不夠嚴密,仍須在酸性高錳酸鉀溶液之前添加洗氣裝置,其理由為.發布:2024/11/19 8:0:1組卷:109引用:4難度:0.5


