在恒壓密閉容器中,充入一定量的H2和CO2發生如下可逆反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,實驗測得反應物在不同溫度下,反應體系中CO2的平衡轉化率與壓強的關系曲線如圖所示。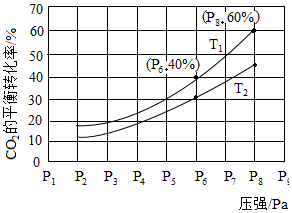
①該反應的△S<<0(填>或<),該反應在低溫低溫(填“低溫”或“高溫”)條件下利于自發進行;
②比較T1與T2的大小關系:T1<<T2(填“<”、“=”或“>”)
③在T1和P6的條件下,往密閉容器中充入3mol H2和1mol CO2,該反應在第5min時達到平衡,此時容器的體積為1.8L;則該反應在此溫度下的平衡常數為427或0.148427或0.148。
4
27
4
27
【考點】轉化率隨溫度、壓強的變化曲線;化學平衡的影響因素.
【答案】<;低溫;<;或0.148
4
27
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:22引用:1難度:0.7
相似題
-
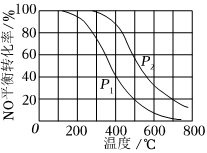 1.一定條件下,將NO(g)和O2(g)按物質的量之比2:1充入反應容器,發生反應:2NO(g)+O2(g)?2NO2(g)。其他條件相同時,分別測得NO的平衡轉化率在不同壓強 (p1、p2)下隨溫度變化的曲線如圖所示。下列說法正確的是( )
1.一定條件下,將NO(g)和O2(g)按物質的量之比2:1充入反應容器,發生反應:2NO(g)+O2(g)?2NO2(g)。其他條件相同時,分別測得NO的平衡轉化率在不同壓強 (p1、p2)下隨溫度變化的曲線如圖所示。下列說法正確的是( )A.p1<p2 B.其他條件不變,溫度升高,該反應的反應限度增大 C.400℃、p1條件下,O2的平衡轉化率為20% D.400℃時,該反應的化學平衡常數的數值為 109發布:2024/12/5 7:30:1組卷:246引用:9難度:0.5 -
 2.向1L的恒容密閉容器中加入1molX和2molY,發生反應:X(g)+2Y(g)?2Z(g),X的轉化率α隨溫度t的變化如圖所示(圖中不同溫度下的轉化率是第5min數據)。下列說法正確的( )
2.向1L的恒容密閉容器中加入1molX和2molY,發生反應:X(g)+2Y(g)?2Z(g),X的轉化率α隨溫度t的變化如圖所示(圖中不同溫度下的轉化率是第5min數據)。下列說法正確的( )A.300℃時,0-5min內平均反應速率v(Z)=0.3mol?L-1?min-1 B.b、c點對應的v逆(Y)大小關系:b>c C.c點時,反應消耗pmolX(p<1),同時消耗2pmolZ D.若將氣體體積縮小為0.5L,則c點溫度下的α(X)減小 發布:2024/12/30 4:0:1組卷:32引用:3難度:0.7 -
 3.在2L的密閉容器中,2A(g)+B(g)?2C(g)ΔH,將2molA氣體和1molB氣體在反應器中反應,測定A的轉化率與溫度的關系如實線圖所示(圖中虛線表示相同條件下A的平衡轉化率隨溫度的變化)。下列說法正確的是( )
3.在2L的密閉容器中,2A(g)+B(g)?2C(g)ΔH,將2molA氣體和1molB氣體在反應器中反應,測定A的轉化率與溫度的關系如實線圖所示(圖中虛線表示相同條件下A的平衡轉化率隨溫度的變化)。下列說法正確的是( )A.反應2A(g)+B(g)?2C(g)的ΔH>0 B.X點的化學平衡常數大于Y點的化學平衡常數 C.圖中Y點v(正)>v(逆) D.圖中Z點,增加B的濃度不能提高A的轉化率 發布:2024/12/30 3:30:1組卷:91引用:7難度:0.5


