甘肅馬家窯遺址出土的青銅刀是我國最早冶煉的青銅器,由于時間久遠,其表面有一層“綠銹”,“綠銹”俗稱“銅綠”,是銅和空氣中的水蒸氣CO2、O2作用產(chǎn)生的,化學式為Cu2(OH)2CO3,“銅綠”能跟酸反應生成銅鹽、CO2和H2O。
(1)物質(zhì)分類標準看,“銅綠”屬于 CC(填字母)。
A.酸
B.堿
C.鹽
D.氧化物
(2)銅器表面有時會生成銅綠,這層銅綠可用化學方法除去,試寫出用鹽酸除去銅綠而不損傷器物的反應的離子方程式 Cu2(OH)2CO3+4H+=2Cu2++2H2O+CO2↑Cu2(OH)2CO3+4H+=2Cu2++2H2O+CO2↑。
(3)古代入們高溫灼孔雀石和木炭的混合物得到一種紫紅色的金屬銅,其化學反應式為CuO+C △ Cu+CO2↑,該反應屬于 BCBC(填序號)。
A.化合反應
B.置換反應
C.氧化還原反應
D.非氧化還原反應
(4)氧化亞銅(Cu2O)是一種鮮紅色粉末狀固體,幾乎不溶于水,可在酸性溶液中發(fā)生反應,與硫酸反應如下:Cu2O+H2SO4═CuSO4+Cu+H2O,該反應中氧化產(chǎn)物為 CuSO4CuSO4。(寫化學式)
(5)Cu2O+4HCl═2HCuCl2+H2O該反應 不是不是(填“是”或“不是”)氧化還原反應。
(6)氧化還原反應中實際上包含氧化和還原兩個過程,下面是一個發(fā)生還原過程的反應式:NO-3+4H++3e-═NO↑+2H2O,將少量Cu2O放入稀硝酸中能使上述還原過程發(fā)生。
①上述反應中生成3個NO分子的同時,轉(zhuǎn)移電子數(shù)目為 99個。
②已知Cu2O被氧化為Cu(NO3)2,寫出Cu2O與稀硝酸反應的化學方程式,并用單線橋標出電子轉(zhuǎn)移的方向和數(shù)目: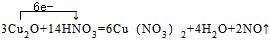
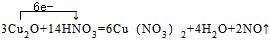 。
。
(7)已知S2-+Br2═S↓+2Br-,2Br-+Cl2═Br2+2Cl-。在含有相同數(shù)目的Na2S和NaBr的溶液中緩慢通入Cl2,下列離子方程式不符合實際情況的是 BB。
A.S2-+Cl2═S↓+2Cl-
B.S2-+2Br-+2Cl2═S↓+Br2+4Cl-
C.2S2-+2Br-+3Cl2═2S↓+Br2+6Cl-
D.3S2-+2Br-+4Cl2═3S↓+Br2+8Cl-
△
NO
-
3
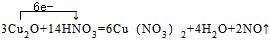
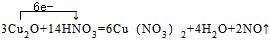
【答案】C;Cu2(OH)2CO3+4H+=2Cu2++2H2O+CO2↑;BC;CuSO4;不是;9;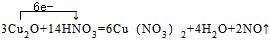 ;B
;B
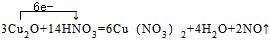 ;B
;B【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:22引用:2難度:0.6
相似題
-
1.下列各組物質(zhì)的分類都正確的是(括號里的是類別)( )
A.空氣(混合物)、C2H5OH(醇)、H2SO4(離子化合物)、液氨(電解質(zhì)) B.CO2(非電解質(zhì))、NH4Cl(銨鹽)、HNO3(含氧酸)、NaOH(強電解質(zhì)) C.HCl(共價化合物)、CH3COOH(羧酸)、Na2O2(堿性氧化物)、CH3I(鹵代烴) D.NO2(酸性氧化物)、CH3CHO(有機物)、CO(有機物)、CH3COOCH3(酯) 發(fā)布:2025/1/4 8:0:1組卷:30引用:3難度:0.9 -
2.下列物質(zhì)分類(或?qū)幕瘜W式)不正確的是( )
A.干冰--氧化物 B.酒精--有機物 C.液氯--Cl2 D.膽礬--CuSO4 發(fā)布:2025/1/4 8:0:1組卷:5引用:1難度:0.9 -
3.下列物質(zhì)分類正確的是( )
A.干冰-氧化物 B.碘酒-單質(zhì) C.純堿-堿 D.葡萄糖-酸 發(fā)布:2025/1/4 8:0:1組卷:16引用:1難度:0.9


