根據如圖1所示實驗,探究酸堿中和反應。

【實驗一】通過溶液酸堿性變化的角度,證明酸堿發生中和反應。
(1)圖①中證明堿與酸發生反應的現象是 溶液由紅色變為無色溶液由紅色變為無色。
(2)圖②中d點溶液中的溶質為 NaCl、HClNaCl、HCl。(填化學式)
【實驗二】通過證明反應物消失的角度,證明酸堿發生中和反應。
(3)當觀察到圖⑤中的現象為 無氣泡產生無氣泡產生時,證明圖④中的酸堿發生了中和反應。
(4)要證明圖④中的酸堿發生了中和反應,還可以選用的物質是 BCBC(填序號)。
A.AgNO3溶液
B.紫色石蕊試液
C.Fe粉
【實驗三】通過導電率變化的角度,證明酸堿發生中和反應。
按如圖2所示裝連接好儀器,在燒杯中加入濃度為c的Ba(OH)2溶液。開啟磁力攪拌器,逐滴滴加相同濃度的稀硫酸,測得溶液的電導率變化曲線如圖3。

【查閱資料】
Ⅰ、室溫下,各物質的電導率數值如表(稀硫酸、Ba(OH)2溶液的濃度相同,設為c)。
| 物質 | 蒸餾水 | 稀硫酸 | Ba(OH)2溶液 | BaSO4懸濁液 |
| 電導率(μS/cm) | 3 | 3921 | 3273 | 3 |
Ⅲ、Ba(OH)2與NaOH具有相似的化學性質。
(5)實驗開始前,測得Ba(OH)2溶液的電導率低于3273μS/cm的原因是
CO2+Ba(OH)2=BaCO3↓+H2O
CO2+Ba(OH)2=BaCO3↓+H2O
(用化學方程式解釋)。(6)反應過程中,電導率最小值可能是
3
3
μS/cm。【考點】中和反應及其應用;溶液的酸堿性與pH的關系.
【答案】溶液由紅色變為無色;NaCl、HCl;無氣泡產生;BC;CO2+Ba(OH)2=BaCO3↓+H2O;3
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:114引用:2難度:0.7
相似題
-
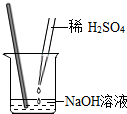 1.小明同學用如圖所示的方法做酸堿中和實驗,采用酚酞試液作指示劑,恰好完全中和時溶液的顏色為( )
1.小明同學用如圖所示的方法做酸堿中和實驗,采用酚酞試液作指示劑,恰好完全中和時溶液的顏色為( )A.無色 B.紅色 C.紫色 D.藍色 發布:2024/12/25 17:0:2組卷:68引用:3難度:0.9 -
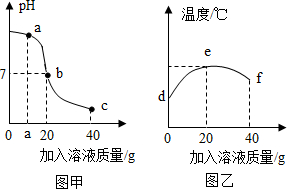 2.某校化學小組在利用鹽酸和氫氧化鈉溶液探究酸堿中和反應時,利用數字化傳感器測得燒杯中溶液pH的變化圖像如圖甲所示,溶液的溫度變化如圖乙所示(不考慮反應過程中熱量損失)。下列說法錯誤的是( )
2.某校化學小組在利用鹽酸和氫氧化鈉溶液探究酸堿中和反應時,利用數字化傳感器測得燒杯中溶液pH的變化圖像如圖甲所示,溶液的溫度變化如圖乙所示(不考慮反應過程中熱量損失)。下列說法錯誤的是( )A.當加入20g氫氧化鈉溶液時恰好完全反應 B.a點時溶液中的溶質為氫氧化鈉和氯化鈉 C.溫度上升是由于中和反應放熱,溫度下降是因為增加液體 D.e點時溶液中的溶質為氯化鈉 發布:2024/12/25 17:0:2組卷:71引用:3難度:0.6 -
3.某研究性學習小組為了探究氫氧化鈉溶液與稀硫酸是否恰好完全反應,分別取少量反應后的溶液于試管中,用下表中的不同試劑進行實驗.下列選項正確的是( )
選項 所用試劑 現象和結論 A 硫酸銅溶液 出現藍色沉淀,則氫氧化鈉過量 B 氯化鋇溶液 出現白色沉淀,則硫酸過量 C 銅絲 有氣泡產生,則硫酸過量 D 無色酚酞溶液 溶液不變色,則恰好完全反應 A.A B.B C.C D.D 發布:2024/12/25 17:30:2組卷:46引用:2難度:0.7


