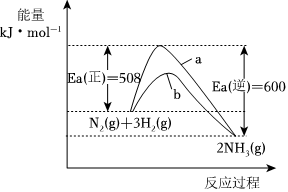
 298.15K時,N2、H2與NH3的平均能量與合成氨反應的活化能的曲線如圖所示,下列說法正確的是( )
298.15K時,N2、H2與NH3的平均能量與合成氨反應的活化能的曲線如圖所示,下列說法正確的是( )
【考點】活化能及其對化學反應速率的影響;有關反應熱的計算.
【答案】C
【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網所有,未經書面同意,不得復制發(fā)布。
發(fā)布:2024/9/15 1:0:9組卷:190引用:2難度:0.7
相似題
-
1.下列對化學反應速率增大原因的分析錯誤的是( )
A.升高溫度,使反應物分子中活化分子百分數增大 B.向反應體系中加入相同濃度的反應物,使活化分子百分數增大 C.對有氣體參加的化學反應,增大壓強使容器容積減小,單位體積內活化分子數增多 D.加入適宜的催化劑,使反應物分子中活化分子百分數增大 發(fā)布:2024/11/9 11:0:1組卷:410引用:17難度:0.6 -
2.關于有效碰撞理論,下列說法正確的是( )
A.活化分子一定能發(fā)生有效碰撞 B.反應物分子之間的碰撞一定會引起化學鍵的斷裂 C.有效碰撞是活化分子在一定的方向上的碰撞 D.發(fā)生有效碰撞的分子具有最高的能量 發(fā)布:2024/8/16 19:0:1組卷:185引用:3難度:0.5 -
3.下列說法正確的是( )
A.反應物分子相互碰撞即能發(fā)生化學反應 B.活化分子之間的碰撞,一定可以發(fā)生化學反應 C.活化分子所具有的能量稱為活化能 D.活化分子百分數越大,反應速率越大 發(fā)布:2024/8/16 20:0:2組卷:22引用:6難度:0.7


