當前位置:
試題詳情
探秘海灘上的物質
在海灘上,你能見到各種各樣的物質,除海洋生物外,最常見的有海沙、貝殼和海水.雖然它們性質和用途各異,但是從元素組成的角度看,這些物質僅是由氧、硅、氯、鉀、鈣等有限的幾種元素組成的.
原子是構成物質的“基石”.一種原子,可以構成最簡單的單質,但更多的是跟其它原子結合成各種化合物,請回答:
[一].從化學的視角認識物質
①海沙是由石英和貝殼小碎片組成,石英的主要成分是(用化學符號表示,下同)SiO2SiO2,貝殼的主要成分是CaCO3CaCO3.
②請寫出一種同時符合下列兩個條件的2種不同類別的化合物的化學式Ca(OH)2Ca(OH)2、H2CO3H2CO3,
(Ⅰ)由氧、硅、氫、碳、鈣五種元素中的三種組成;
(Ⅱ)按組成分類,與①中兩種物質的主要成分類別不同.
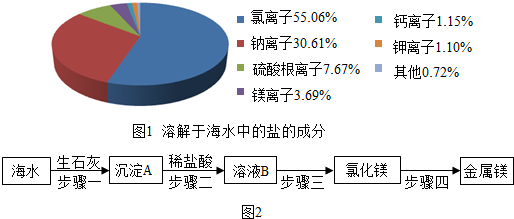
③海水中含有多種無機鹽,各離子的含量如圖1所示.請寫出構成硫酸鎂的微粒符號:Mg2+、SO42-Mg2+、SO42-.假設海水中無機鹽的含量為3.5%,鎂離子全部以氯化鎂的形式存在,則Wg海水中含有氯化鎂質量的計算公式為:Wg×3.5%×3.69%×9524Wg×3.5%×3.69%×9524.
④食用低鈉鹽可預防高血壓,低鈉鹽是在氯化鈉中添加了適量的氯化鉀,氯化鉀除了有咸味外,還帶有苦味,從物質構成的角度看,氯化鉀有苦味可能是鉀離子鉀離子造成的.
[二].用化學的方法改造物質
(1)海水中含有豐富的鎂元素,目前大多數金屬鎂是從海水中提取的,其生產流程如下(如圖2):
①請寫出步驟一和步驟二反應的化學方程式.
步驟一:CaO+H2O=Ca(OH)2CaO+H2O=Ca(OH)2、Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2;
步驟二:Mg(OH)2+2HCl=MgCl2+2H2OMg(OH)2+2HCl=MgCl2+2H2O;
②在步驟一中,分離出沉淀A的方法是過濾過濾,在實驗室中進行此項操作,除燒杯外,還需要的玻璃儀器有漏斗、玻璃棒漏斗、玻璃棒.
(2)太陽能光伏發電最關鍵的材料是高純硅,生產高純硅的流程示意圖如下(如圖3):

發生的反應為:①SiO2+2C 高溫 Si+2CO↑ ②Si+3HCl △ SiHCl3+H2
③SuHCl2+H2 高溫 Si+3HCl
①整個制備過程必須達到無水無氧,在H2還原SiHCl3過程中若混入O2,可能引起的后果是Si會被再次氧化,得不到純凈的Si,易引起爆炸Si會被再次氧化,得不到純凈的Si,易引起爆炸.
②為了達到綠色化學和節約資源的目的,上述流程中某化合物需要循環使用,該物質的化學式是HClHCl.
W
g
×
3
.
5
%
×
3
.
69
%
×
95
24
W
g
×
3
.
5
%
×
3
.
69
%
×
95
24
高溫
△
高溫
【答案】SiO2;CaCO3;Ca(OH)2;H2CO3;Mg2+、SO42-;;鉀離子;CaO+H2O=Ca(OH)2;Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2;Mg(OH)2+2HCl=MgCl2+2H2O;過濾;漏斗、玻璃棒;Si會被再次氧化,得不到純凈的Si,易引起爆炸;HCl
W
g
×
3
.
5
%
×
3
.
69
%
×
95
24
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/10/31 8:0:1組卷:13引用:1難度:0.5
相似題
-
1.閩東的淡水和海水資源豐富
(1)興趣小組測量集中水樣的pH,得到下表數據,其中堿性最強的是(填序號)
(2)山泉水含有較多鈣、鎂離子,硬度較高水樣 來源 pH A 泉水:“海上仙都”-太姥山 6.8~7.0 B 河水:“海國桃園”-楊家溪 7.2~7.6 C 海水:“天然良港”-三都澳 7.8~8.0
①寫出鈣離子的符號
②若要降低其硬度,可采用的方法是(寫一種)
(3)海水是重要資源,處理的大致流程如圖: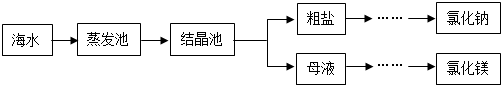
①粗鹽經過溶解、過濾、蒸發可除去海沙等不溶性雜質.
a.海沙的主要成分是二氧化硅(SiO2),其中Si的化合價為.
b.若以上操作在實驗室中進行,溶解時,玻璃棒的作用是.
②母液經過處理,可得氯化鎂,點解熔融氯化鎂生成鎂和氯氣(Cl2).寫出電解氯化鎂的化學方程式:.發布:2024/12/22 8:0:1組卷:13引用:1難度:0.5 -
2.我國的領海主權不容侵犯,南海是我國的固有領海,蘊藏著豐富的海洋資源。
(1)南海不僅蘊含著大量的煤、石油、天然氣等常規能源,還蘊藏著大量的可燃冰。可燃冰(主要成分是CH4)被科學家譽為“未來能源”,CH4燃燒的化學方程式,可燃冰作為能源與煤、石油相比的優點是。
(2)南海某島采用風力發電提供的電能對海水進行了如圖1所示的綜合利用。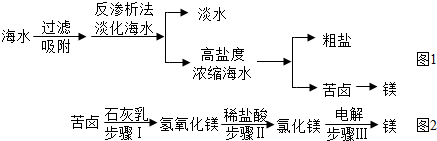
①反滲析法淡化海水是利用海水中各成分的不同分離出淡水。
②將高鹽度濃縮海水進行可以分離得到粗鹽。
③用苦鹵制取金屬鎂的流程圖如圖2:
上述轉化過程中,所發生的反應屬于復分解反應類型的步驟是(填序號),步驟Ⅱ的化學方程式為。利用苦鹵制取氫氧化鎂比“直接向海水中加入石灰乳制取氫氧化鎂”的優勢是。
(3)如圖3是海水“制堿”的部分簡單流程。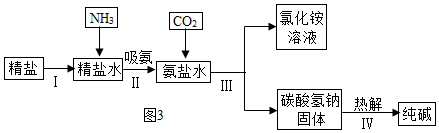
①步驟IⅡ反應的化學方程式為;
②制氨鹽水的過程中要先通入氨氣,再通入二氧化碳,如果反過來,二氧化碳的吸收率會降低,這是因為;
③氨鹽水吸收二氧化碳后生成碳酸氫鈉和氯化銨,首先析出的物質是,原因是,將氯化銨溶液和碳酸氫鈉固體分離的方法是過濾,濾液中的溶質有。發布:2024/12/25 12:0:1組卷:85引用:4難度:0.6 -
3.海洋是人類巨大的資源寶庫,其中含有的可溶性物質包括MgCl2等。如圖為從海水中提取金屬鎂的簡易流程圖。

(1)海洋中含量最多的物質是。
(2)貝殼煅燒的化學方程式是。
(3)操作Ⅰ的名稱是,進行該操作時,用到的玻璃儀器有燒杯、玻璃棒和。其中玻璃棒的作用是。
(4)生石灰轉化為石灰乳的過程是反應(選填“吸熱”或“放熱”)。
(5)寫出氫氧化鎂和鹽酸反應的化學方程式。
(6)上述流程中未涉及到的基本反應類型是反應。發布:2024/12/24 12:0:2組卷:221引用:4難度:0.2


