研究含氮、硫物質之間的轉化,對資源的綜合利用具有重要意義。
(1)硫酸生產中,SO2催化氧化生成SO3:2SO2(g)+O2(g)?2SO3(g)ΔH=-196.6kJ?mol-1
①在恒容密閉容器中達到平衡后,能使平衡正向移動并提高SO2轉化率的是 ADAD。
A.向容器中通入O2
B.向容器中通入SO2
C.使用催化劑
D.降低溫度
②如圖1表示SO2催化氧化生成SO3在密閉容器中達到平衡時,由于條件改變而引起反應速率的變化情況,a時刻改變的條件可能是 升溫升溫;若c時刻增大壓強,把反應速率變化情況畫在c~d處 
 。
。
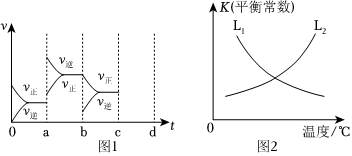
(2)合成氨反應N2(g)+3H2(g)?2NH3(g)ΔH<0是人工固氮的主要手段,對人類生存和經(jīng)濟發(fā)展都有著重大意義。合成氨反應中正反應速率v正=k正c(N2)?c3(H2),逆反應速率v逆=k逆c2(NH3)。k正、k逆為速率常數(shù)。平衡常數(shù)K與溫度的關系如圖2。
①表示正反應的平衡常數(shù)K與溫度變化的曲線為 L1L1(填L1或L2)。
②平衡時,合成氨反應的平衡常數(shù)K=k正k逆k正k逆(用k正、k逆表示)。
(3)將一定量N2O4氣體充入恒容的密閉容器中,控制反應溫度為T1,發(fā)生的反應為:N2O4(g)?2NO2(g)ΔH>0。
①下列可作為反應達到平衡的判據(jù)是 BDBD。
A.V正(N2O4)=2v逆(NO2)
B.氣體的壓強不變
C.ΔH不變
D.容器內顏色不變
②時刻反應達到平衡,混合氣體平衡總壓強為P,N2O4的平衡轉化率為80%,則反應N2O4(g)?2NO2(g)的平衡常數(shù)Kp=649P649P(用平衡分壓代替平衡濃度,分壓=總壓×物質的量分數(shù))。


k
正
k
逆
k
正
k
逆
64
9
64
9
【答案】AD;升溫; ;L1;;BD;P
;L1;;BD;P
 ;L1;
;L1;k
正
k
逆
64
9
【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:36引用:3難度:0.6
相似題
-
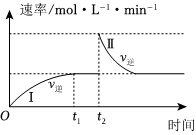 1.在某一恒溫體積可變的密閉容器中發(fā)生反應:X(g)+Y(g)?2Z(g) ΔH<0。t1時刻達到平衡后,在t2時刻改變某一條件,其反應過程如圖所示。下列說法正確的是( )
1.在某一恒溫體積可變的密閉容器中發(fā)生反應:X(g)+Y(g)?2Z(g) ΔH<0。t1時刻達到平衡后,在t2時刻改變某一條件,其反應過程如圖所示。下列說法正確的是( )A.t2時刻改變的條件是向密閉容器中加Z B.0~t2時,v正>v逆 C.Ⅰ、Ⅱ兩過程達到平衡時,X的體積分數(shù)Ⅰ>Ⅱ D.Ⅰ、Ⅱ兩過程達到平衡時,平衡常數(shù)Ⅰ<Ⅱ 發(fā)布:2024/9/28 0:0:2組卷:23引用:3難度:0.5 -
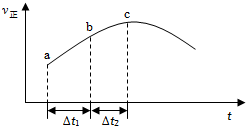 2.SO2(g)+NO2(g)?SO3(g)+NO(g),向容器中投入一定量的SO2和NO2發(fā)生反應,正反應速率隨時間變化的示意圖如圖所示。下列說法正確的是( )
2.SO2(g)+NO2(g)?SO3(g)+NO(g),向容器中投入一定量的SO2和NO2發(fā)生反應,正反應速率隨時間變化的示意圖如圖所示。下列說法正確的是( )A.反應物濃度:a點小于b點 B.反應物的總能量大于生成物的總能量 C.SO2的轉化率:a>b>c D.反應進行到c點達平衡 發(fā)布:2024/11/27 3:0:1組卷:84引用:2難度:0.5 -
3.某研究小組探究外界條件對化學反應mA(g)+nB(g)?pC(g)的速率和平衡的影響,如圖所示。下列判斷正確的是( )
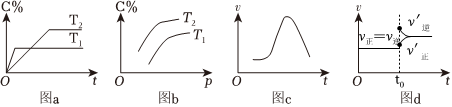
A.由圖a可知,T1>T2,該反應的正反應為吸熱反應 B.由圖b可知,該反應m+n<p C.若圖c是絕熱條件下速率和時間的圖像,則該反應是放熱反應 D.由圖d可知,t0時刻充入了一定量的C 發(fā)布:2024/10/11 9:0:2組卷:61引用:2難度:0.7


