化學是一門研究物質的科學,我們一般從物質的存在、性質、制備、用途等方面研究一種物質或一類物質。以金屬為例,請你參與其中回答相關問題:
(1)認識金屬元素存在:自然界中大多數金屬都以化合物的形式存在。下列礦石的主要成分屬于氧化物的是 ADAD(填字母序號);
A.鋁土礦(主要成分Al2O3)
B.輝銅礦(主要成分Cu2S)
C.菱鐵礦(主要成分FeCO3)
D.磁鐵礦(主要成分Fe3O4)
(2)探究金屬物理性質:下表是A、B、C三種金屬的部分物理性質。
| 金屬 | 導電性(100為標準) | 密度(g/cm3) | 熔點(℃) | 硬度(10為標準) |
| A | 99 | 8.92 | 1083 | 3 |
| B | 61 | 2.70 | 660 | 2.9 |
| C | 17 | 7.86 | 1535 | 5 |
金屬B的密度比A小
金屬B的密度比A小
。②C的合金通常可以做菜刀、錘子等,其合金的硬度
>
>
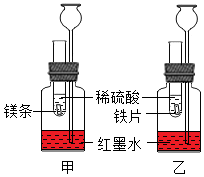
5(填“>”“<”或“=”)。(3)探究金屬化學性質及反應規律:在室溫條件下進行如圖所示實驗。若實驗中各種條件均相同,觀察到甲中的長頸漏斗內紅墨水柱比乙高,試解釋產生這種現象的原因
反應時鎂比鐵放出的熱量多
反應時鎂比鐵放出的熱量多
。
(4)認識金屬的制備:我國西漢時期就有“曾青得鐵則化為銅”的記載,其中蘊涵的濕法冶銅原理為:
Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
(用化學方程式表示)。(5)金屬在生產生活中應用廣泛。如圖,向一定量硝酸銀溶液中加入銅和鋅的混合粉末,充分反應后過濾,得溶液甲和固體乙。
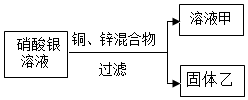
①若乙中含有鋅、銅、銀三種固體,此時向固體乙中加入稀鹽酸,發生反應的化學方程式為
Zn+2HCl=ZnCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
。②若溶液甲顯藍色,是因為
Cu+2AgNO3=Cu(NO3)2+2Ag
Cu+2AgNO3=Cu(NO3)2+2Ag
(用化學反應方程式表示),此時固體乙中一定含有的物質是銀
銀
。(6)某煉鐵廠用赤鐵礦石冶煉生鐵。用2000t含氧化鐵80%的赤鐵礦礦石理論上可以煉出含鐵96%生鐵多少噸?
【答案】AD;金屬B的密度比A小;>;反應時鎂比鐵放出的熱量多;Fe+CuSO4=FeSO4+Cu;Zn+2HCl=ZnCl2+H2↑;Cu+2AgNO3=Cu(NO3)2+2Ag;銀
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:27引用:1難度:0.4
相似題
-
 1.隨著經濟的發展,能源、環境、材料成為人們日益關注的問題:
1.隨著經濟的發展,能源、環境、材料成為人們日益關注的問題:
(1)倡導“低碳”生活,保護環境,下列舉措能達到“低碳”目的是。
A.提倡使用節能燈
B.廣泛使用一次性筷子
C.利用和開發太陽能、風能等能源
D.選擇步行、騎自行車等方式出行
(2)工業上,用一氧化碳還原含有氧化鐵80%的鐵礦石,可以得到560t的鐵,求鐵礦石的質量。(寫出計算過程)
(3)高速鐵路可以加快出行步伐。結合所學化學知識,回答下列問題:
I、圖中標示的物質中為金屬材料的是(填序號),生鐵和鋼的區別是。
Ⅱ、修建鐵路所需的大量鋼鐵是以鐵礦石為主要原料冶煉而得。下列礦石的主要成分屬于氧化物的是(填字母序號)。
A.鋁土礦(主要成分Al2O3)
B.輝銅礦(主要成分Cu2S)
C.菱鐵礦(主要成分FeCO3)
D.磁鐵礦(主要成分Fe3O4)
Ⅲ、高鐵酸鈉(Na2FeO4)是高鐵列車上常用的一種“綠色環保高效”消毒劑。高鐵酸鈉中鐵元素化合價為。發布:2024/11/6 8:0:1組卷:28引用:1難度:0.6 -
2.現在的鞍鋼集團是世界第三大鋼鐵公司,是涵蓋礦石開采、鋼鐵煉制,鋼鐵加工全產業鏈的大型鋼鐵聯合企業,重組本鋼后,公司有望實現年產粗鋼7000Wt(萬噸),產鐵精礦5000Wt的戰略目標。假設粗鋼中含鐵98%,鐵精礦中Fe2O3含量為90%(其他為不含鐵的雜質)。請計算:
(1)Fe2O3中鐵的質量分數為。(不書寫計算過程,計算結果保留至1%)
(2)現今鞍鋼集團鐵礦石的自給率?(礦石自給率是指企業自產礦石占企業所需礦總量的百分比,請依據化學方程式計算并書寫計算過程,計算結果保留至1%)發布:2024/11/13 23:0:1組卷:96引用:2難度:0.5 -
3.金屬和金屬化合物的用途廣泛,是初中化學學習的重要內容.
(1)下列關于合金的說法中錯誤的是.
a.合金是混合物
b.合金中不能含非金屬元素
c.生鐵和鋼都屬于合金
d.合金比純金屬應用更廣泛
(2)國家大劇院安裝了近2萬塊鈦合金板,其密度只有鋼的60%.生產金屬鈦可用置換法,即將四氯化鈦與金屬鎂在高溫狀態下發生置換反應,則反應的化學方程式為.
(3)某實驗室廢液缸里的廢液含有CuSO4、ZnSO4、FeSO4,如果將廢液直接排放就會造成水污染,化學小組利用課余時間處理廢液,回收工業原料硫酸鋅和有關金屬.實驗過程如圖1.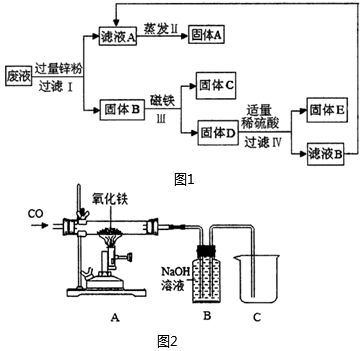
①過濾、蒸發操作中都用到的儀器是;
②固體C的化學式為;
③最終所得硫酸鋅的質量(填“大于”、“小于”或“等于”)原廢液中硫酸鋅質量.
(4)圖2是化學小組設計的工業煉鐵模擬實驗裝置.
①反應結束后,請設計實驗證明裝置B中的溶液還含有NaOH(簡要寫出操作、現象和結論);
②請說明該實驗不需要增加尾氣處理裝置的理由;
③現有2000t含氧化鐵80%的赤鐵礦,可冶煉出多少噸含雜質為4%的生鐵(準確到0.1)?發布:2024/12/31 8:0:1組卷:51引用:1難度:0.5


