圖中X、Y、Z為單質(zhì),其他為化合物,它們之間存在如下轉(zhuǎn)化關(guān)系(部分產(chǎn)物已略去).其中,A俗稱磁性氧化鐵;E是不溶于水的酸性氧化物,能與氫氟酸反應(yīng).

回答下列問(wèn)題:
(1)組成單質(zhì)Z的元素在周期表中的位置是第三周期IVA族第三周期IVA族; R的化學(xué)式是H2SiO3H2SiO3;
(2)E、Z的晶體類型均屬于原子原子晶體.E、Z結(jié)構(gòu)中最小的環(huán)上原子個(gè)數(shù)之比為2:12:1.B為一元強(qiáng)堿,焰色反應(yīng)為紫色,則B的電子式為
 .
.
(3)寫(xiě)出下列反應(yīng)的化學(xué)方程式:
①單質(zhì)Z與 NaOH的反應(yīng):Si+2NaOH+H2O=Na2SiO3+2H2↑Si+2NaOH+H2O=Na2SiO3+2H2↑
②工業(yè)上由E制取粗Z:SiO2+2C 高溫 Si+2CO↑SiO2+2C 高溫 Si+2CO↑
(4)已知A與1mol Al反應(yīng)轉(zhuǎn)化為X時(shí)(所有物質(zhì)均為固體),放出a kJ 熱量,寫(xiě)出該反應(yīng)的熱化學(xué)方程式:8Al(s)+3Fe3O4(s)=9Fe(s)+4Al2O3(s)△H=-8a kJ/mol8Al(s)+3Fe3O4(s)=9Fe(s)+4Al2O3(s)△H=-8a kJ/mol.
(5)向A與X的混合物中加入100mL 1mol/L鹽酸恰好使混合物完全溶解,放出標(biāo)準(zhǔn)狀況下的氣體224mL,在溶液中加入KSCN溶液無(wú)血紅色出現(xiàn).若用足量的CO在高溫下還原相同質(zhì)量的混合物,能得到單質(zhì)的質(zhì)量為2.8g2.8g.


高溫
高溫
【考點(diǎn)】無(wú)機(jī)物的推斷.
【答案】第三周期IVA族;H2SiO3;原子;2:1; ;Si+2NaOH+H2O=Na2SiO3+2H2↑;SiO2+2C Si+2CO↑;8Al(s)+3Fe3O4(s)=9Fe(s)+4Al2O3(s)△H=-8a kJ/mol;2.8g
;Si+2NaOH+H2O=Na2SiO3+2H2↑;SiO2+2C Si+2CO↑;8Al(s)+3Fe3O4(s)=9Fe(s)+4Al2O3(s)△H=-8a kJ/mol;2.8g
 ;Si+2NaOH+H2O=Na2SiO3+2H2↑;SiO2+2C
;Si+2NaOH+H2O=Na2SiO3+2H2↑;SiO2+2C高溫
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書(shū)面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:21引用:4難度:0.5
相似題
-
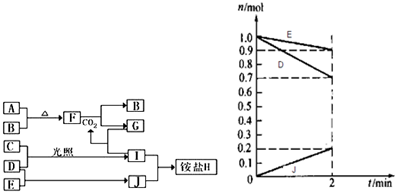
1.如圖是部分短周期元素的單質(zhì)及其化合物(或其溶液)的轉(zhuǎn)化關(guān)系,已知B、C、D、E是非金屬單質(zhì),且在常溫常壓下都是氣體;化合物G的焰色反應(yīng)為黃色,化合物I和J通常狀況下呈氣態(tài);
請(qǐng)完成下列填空:
(1)H的化學(xué)式;其晶體中所含化學(xué)鍵類型為;檢驗(yàn)H 中陽(yáng)離子的方法是.
(2)A與B 在加熱條件下反應(yīng)的主要現(xiàn)象是;F和H2O反應(yīng)的化學(xué)方程式為;寫(xiě)出G溶液中加入過(guò)量的I溶液反應(yīng)的離子方程式.
(3)某溫度時(shí),在2L容器中,D、E、J三種物質(zhì)的物質(zhì)的量隨時(shí)間變化的曲線如圖所示.由圖中數(shù)據(jù)分析:該反應(yīng)的化學(xué)方程式為.反應(yīng)開(kāi)始至2min,用J表示的平均反應(yīng)速率為.發(fā)布:2024/12/30 15:0:1組卷:6引用:3難度:0.3 -
2.已知某物質(zhì)X 能發(fā)生如下轉(zhuǎn)化:X
YO2①ZO2②A。下列有關(guān)上述轉(zhuǎn)化關(guān)系中物質(zhì)及其反應(yīng)的敘述錯(cuò)誤的是( )H2O③A.若X為NH3,則A為硝酸 B.若X為H2S,則A為亞硫酸或者硫酸 C.反應(yīng)①和②一定為氧化還原反應(yīng),反應(yīng)③有可能為非氧化還原反應(yīng) D.若X為非金屬單質(zhì)或非金屬氫化物,則A 一定能與金屬銅反應(yīng)生成Y 發(fā)布:2025/1/6 6:0:5組卷:28引用:2難度:0.5 -
3.通常情況下,微粒A和B為分子,C和E為陽(yáng)離子,D為陰離子,它們都含有10個(gè)電子;B溶于A后所得的物質(zhì)可電離出C和D;A、B、E三種微粒反應(yīng)后可得C和一種白色沉淀.請(qǐng)回答.
(1)用化學(xué)符號(hào)表示下列微粒:C:,D:.
(2)寫(xiě)出A、B、E三種微粒反應(yīng)的離子方程式:.發(fā)布:2024/12/30 17:0:2組卷:48引用:19難度:0.5


