從古至今,鐵及其化合物一直被人類廣泛應用。
(一)鐵及其化合物的應用
(1)明代科學著作《天工開物》中記載:“泥固塞其孔,然后使水轉釉”是指高溫下CO將紅磚中的Fe2O3轉化為Fe3O4而形成青磚。該轉化的化學方程式為 3Fe2O3+CO 高溫 2Fe3O4+CO23Fe2O3+CO 高溫 2Fe3O4+CO2。
(2)鐵的化合物在現代更多領域發揮著重要作用。
①碳酸亞鐵(FeCO3)不溶于水,可作補血劑,服用后與胃酸反應生成 氯化亞鐵氯化亞鐵被人體吸收,促進血紅蛋白的生成。
②火星探測器發回的信息表明,火星上存在FeOOH,從而證明火星表面曾經存在過水,其理由為 FeOOH中存在H、O元素FeOOH中存在H、O元素。
③活性FeOOH可除去石油開采過程中的有害氣體H2S,并獲得S,原理如下。
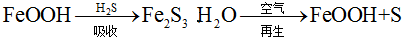
吸收中生成的另一種物質的化學式為 H2OH2O,再生時發生反應的化學方程式為 2(Fe2S3?H2O)+3O2=4FeOOH+6S2(Fe2S3?H2O)+3O2=4FeOOH+6S。
(二)FeOOH的制備
用廢鐵屑(主要成分為Fe,含少量Fe2O3和FeCO3)制備FeOOH主要流程如下。
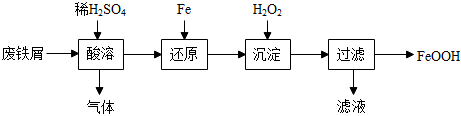
(3)酸溶時適當提高反應溫度和H2SO4濃度,目的是 加快反應速率加快反應速率,產生的氣體為 氫氣和二氧化碳氫氣和二氧化碳。
(4)還原發生的反應為Fe2(SO4)3+Fe═3FeSO4。
沉淀發生的反應為2FeSO4+H2O2+2H2O═2FeOOH↓+2H2SO4。
沉淀時反應溫度不宜太高,原因是 防止過氧化氫受熱分解防止過氧化氫受熱分解。
(三)FeOOH的含量測定
已知:FeOOH及鐵的氧化物加熱分解的溫度如下。
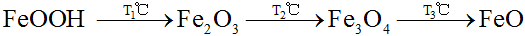
稱取含Fe3O4的FeOOH樣品76.6g,進行熱分解實驗。控制不同的溫度對樣品加熱,測得剩余固體質量隨溫度的變化如圖所示。
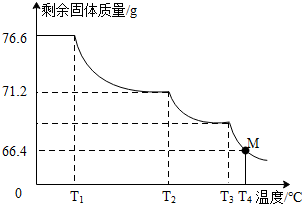
(5)樣品中FeOOH的含量為 69.769.7%(精確到0.1%)。
(6)當加熱到T4℃時,M點固體的成分是 Fe3O4和FeOFe3O4和FeO。
高溫
高溫
【答案】3Fe2O3+CO 2Fe3O4+CO2;氯化亞鐵;FeOOH中存在H、O元素;H2O;2(Fe2S3?H2O)+3O2=4FeOOH+6S;加快反應速率;氫氣和二氧化碳;防止過氧化氫受熱分解;69.7;Fe3O4和FeO
高溫
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:98引用:2難度:0.5
相似題
-
1.新冠肺炎疫情防控期間,西安市各學校開展全域噴灑低濃度、有效成分是次氯酸鈉的“84”消毒液進行消毒。如圖所示是模擬制備“84”消毒液的流程(Cl2是一種黃綠色的有毒氣體)。請回答下列問題:
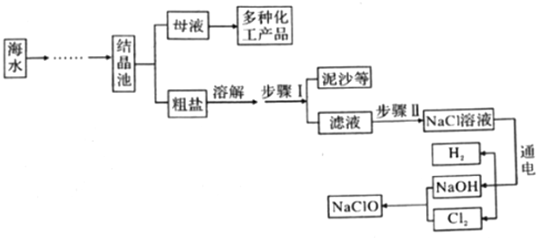
(1)NaOH的俗稱為(寫一種)。
(2)步驟Ⅱ中,通常用碳酸鈉溶液除去濾液中的氯化鈣雜質,請寫出有關反應的化學方程式。
(3)電解水時,一般在水中加入少量NaOH以增強水的導電性,不能加入NaCl的原因是。發布:2025/1/3 8:0:1組卷:6引用:1難度:0.5 -
2.某種家用的消毒液的主要成分是次氯酸鈉(NaClO),制取NaClO的化學方程式為:Cl2+2NaOH=NaClO+NaCl+H2O,下列說法錯誤的是( )
A.NaClO中氯元素的化合價為-1 B.反應中用到的NaOH俗稱燒堿 C.該化學方程式中涉及到兩種鹽 D.反應前后氯元素化合價既升高又降低 發布:2025/1/3 8:0:1組卷:71引用:1難度:0.7 -
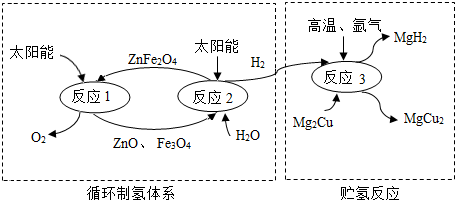 3.如圖是制取與貯存氫氣的一種方法,Mg2Cu是一種貯氫合金,吸氫后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列說法不正確的是( )
3.如圖是制取與貯存氫氣的一種方法,Mg2Cu是一種貯氫合金,吸氫后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列說法不正確的是( )A.ZnFe2O4中Fe的化合價為+3價 B.循環制氫反應中無需加入ZnFe2O4 C.反應1和反應2的總方程式為:2H2O 2H2↑+O2↑通電D.M與足量稀鹽酸反應生成的H2質量大于反應2產生的H2質量 發布:2024/12/31 8:0:1組卷:48引用:2難度:0.5


