某學(xué)習(xí)小組開展了“設(shè)計和制作簡易供氧器”的實踐活動。已知某品牌制氧機的制氧劑為過碳酸鈉和二氧化錳,是過氧化氫與碳酸鈉的加合物,遇水后能產(chǎn)生氧氣,放出熱量。
 ?
?
【活動一】認(rèn)識制氧機
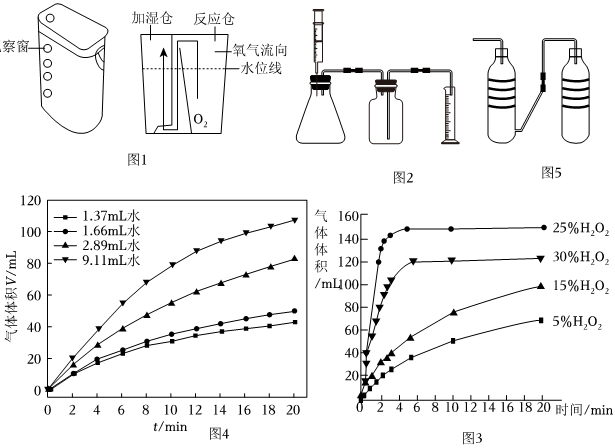
(1)制氧機如圖1所示:外殼上留有觀察窗,以便觀察氧氣的產(chǎn)生速率和反應(yīng)進程。制氧倉是反應(yīng)倉,是氧氣產(chǎn)生的場所。過濾加濕倉起到的作用是 ABCDABCD。
A.洗氣作用,濾去氧氣中的各種雜質(zhì),通過洗滌確保氧氣的純度
B.降低反應(yīng)溫度,使反應(yīng)能夠平穩(wěn)進行
C.使產(chǎn)生的氧氣具有一定的濕度,適合人們呼吸
D.通過氣泡觀察氧氣生成的速率
E.加快生成氧氣的速率
【活動二】選擇制氧劑
過氧化氫也可以快速產(chǎn)生氧氣,為什么不選擇過氧化氫?過碳酸鈉是碳酸鈉和過氧化氫的加成化合物,它的制氧效率是否優(yōu)于過氧化氫?于是該興趣小組對兩者的制氧效率進行探究,并篩選合適的制氧劑。
實驗一:過氧化氫作為制氧劑
小組設(shè)計了圖2實驗裝置,用表1中等質(zhì)量的過氧化氫進行實驗。在集氣瓶中加滿水,錐形瓶中加入0.2g二氧化錳,注入雙氧水,記錄并處理20min內(nèi)數(shù)據(jù)如圖3所示。
表1
| 編號 | 濃度/% | 體積/mL |
| ① | 5 | 9.11 |
| ② | 15 | 2.89 |
| ③ | 25 | 1.66 |
| ④ | 30 | 1.37 |
過氧化氫水+氧氣
二氧化錳
過氧化氫水+氧氣
,其中二氧化錳的作用是 二氧化錳
催化作用
催化作用
。(3)20min時,④比③產(chǎn)氧量少,可能的原因是
反應(yīng)放出大量熱,使反應(yīng)物減少
反應(yīng)放出大量熱,使反應(yīng)物減少
。(4)已知:高濃度過氧化氫易揮發(fā)且腐蝕性強。因此可以選擇濃度為
5%
5%
的過氧化氫溶液作為制氧劑。實驗二:過碳酸鈉作為制氧劑
往錐形瓶中加入1.41g過碳酸鈉、0.2g二氧化錳和VmL水,待反應(yīng)完全后收集到約159.1mL水(產(chǎn)生氧氣的量與上表中藥品得到氧氣的最大量相等)。其它藥品質(zhì)量不變,再分別用不同體積的水進行實驗。記錄并處理20min內(nèi)數(shù)據(jù)如圖4。
(5)V=
9.11
9.11
mL。(6)由圖4可得出的結(jié)論是
產(chǎn)氧速率隨加水量的增加而增大
產(chǎn)氧速率隨加水量的增加而增大
。(7)結(jié)合圖3、圖4中數(shù)據(jù)分析,前2min過碳酸鈉與過氧化氫的制氧效率相當(dāng),分析圖3、圖4中2min后的數(shù)據(jù),選擇過碳酸鈉的依據(jù)是
過碳酸鈉產(chǎn)氧速率比過氧化氫產(chǎn)氧速率快
過碳酸鈉產(chǎn)氧速率比過氧化氫產(chǎn)氧速率快
。(8)制氧劑不選擇過氧化氫溶液,還因為
ABD
ABD
(填字母)。A.過碳酸鈉是顆粒物,易于保存
B.過氧化氫運輸儲存不方便
C.過氧化氫分解產(chǎn)物無污染
D.過氧化氫濃度較大時,具有腐蝕性
【活動三】制作供氧器
(9)學(xué)習(xí)小組利用身邊物品自制了如圖5的簡易供氧器。與真實產(chǎn)品對比中,形成的觀點不正確的是
A
A
(填字母)。A.產(chǎn)氧和洗氣裝置組合不用一體化
B.內(nèi)部氣體流向采用高進低出方式
C.特定需求是選擇制氧方法的重要依據(jù)
D.制氧機要符合美學(xué)、工程、安全等標(biāo)準(zhǔn)
【答案】ABCD;過氧化氫水+氧氣;催化作用;反應(yīng)放出大量熱,使反應(yīng)物減少;5%;9.11;產(chǎn)氧速率隨加水量的增加而增大;過碳酸鈉產(chǎn)氧速率比過氧化氫產(chǎn)氧速率快;ABD;A
二氧化錳
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/9/16 2:0:9組卷:85引用:2難度:0.5
相似題
-
1.學(xué)習(xí)小組開展了“設(shè)計和制作簡易供氧器”的實踐活動。
某品牌制氧機的制氧劑為過碳酸鈉(化學(xué)式2Na2CO3?3H2O2,白色固體)和二氧化錳。制氧過程的反應(yīng)為:過碳酸鈉碳酸鈉+水+氧氣,該反應(yīng)為放熱反應(yīng)。二氧化錳
【活動一】認(rèn)識制氧機
(1)觀察窗的作用是。
(2)加濕倉的作用是。
【活動二】選擇制氧劑
實驗一:過氧化氫
小組設(shè)計了如圖2實驗裝置,用表中質(zhì)量相等的四組過氧化氫溶液進行實驗。在集氣瓶中加滿水,錐形瓶中加入0.2gMnO2注入溶液,記錄并處理20min內(nèi)數(shù)據(jù)如圖3。
(3)反應(yīng)的文字表達式為編號 ① ② ③ ④ 濃度/% 5 15 25 30 體積/mL 9.11 9.11 1.66 1.37 。
(4)④比③產(chǎn)氧量少,可能的原因是。
實驗二:過碳酸鈉
往錐形瓶中加入1.4g過碳酸鈉、0.2gMnO2和9.11mL水,待反應(yīng)完全后收集到約159.1mL水,(產(chǎn)生氧氣的量與上表中藥品得到氧氣的最大量相等)。其它藥品質(zhì)量不變,再分別用不同體積的水進行實驗。記錄并處理20min內(nèi)數(shù)據(jù)如圖4。
(5)由圖4可得出的結(jié)論是。
【活動三】制作供氧器
(6)綜合分析,選用過碳酸鈉作制氧劑的理由是。
(7)學(xué)習(xí)小組利用身邊物品自制了如圖5的簡易供氧器,與真實產(chǎn)品對比中,形成的觀點不正確的是(填字母)。
A.產(chǎn)氧和洗氣裝置組合不用一體化
B.內(nèi)部氣體流向采用高進低出方式
C.特定需求是選擇制氧方法的重要依據(jù)
D.制氧機要符合美學(xué)、工程、安全等標(biāo)準(zhǔn)發(fā)布:2024/9/12 2:0:8組卷:38引用:1難度:0.5 -
2.學(xué)習(xí)小組開展了“設(shè)計和制作簡易供氧器”的實踐活動。如圖家用“氧立得”牌制氧機。

制氧劑試劑:過氧化氫溶液、二氧化錳、過氧化鈉、過碳酸鈉等。
【閱讀資料】
①過氧化氫制氧氣:過氧化氫在二氧化錳催化下生成水和氧氣,并放出熱量。
②過碳酸鈉制氧氣:過碳酸鈉溶于水生成碳酸鈉和過氧化氫,過氧化氫在二氧化錳催化下生成水和氧氣。該反應(yīng)過程下能持續(xù)放出高純氧氣并放熱。
③過碳酸鈉是白色固體,化學(xué)式為:2Na2CO3?3H2O2
【活動一】認(rèn)識制氧機
(1)觀察窗的作用是。
(2)加濕倉的作用是。
【活動二】選擇制氧劑
實驗一:過氧化氫
小組設(shè)計圖2實驗裝置,用不同濃度的四組過氧化氫溶液進行實驗。在集氣瓶中加滿水,錐形瓶中加入0.2gMnO2,注入溶液,記錄并處理20min內(nèi)數(shù)據(jù)如圖3。
(3)檢查圖2裝置氣密性的操作是。(假設(shè)導(dǎo)管末端口堵住)
(4)過氧化氫制氧氣的文字表達式。
(5)分析圖3中30%H2O2比25%H2O2產(chǎn)氧量少,可能的原因是。
實驗二:過碳酸鈉
往錐形瓶中加入一定量的過碳酸鈉、0.2gMnO2,再分別用不同體積的水進行實驗。記錄并處理20min內(nèi)數(shù)據(jù)如圖4。
(6)過碳酸鈉:2Na2CO3?3H2O2屬于(選填“混合物”或“純凈物”)。
(7)由圖4可得出的結(jié)論是。
【活動三】制作供氧器
(8)綜合分析,選用過碳酸鈉作制氧劑的理由是。
(9)學(xué)習(xí)小組利用身邊物品自制了如圖5的簡易供氧器。與真實產(chǎn)品對比中,形成的觀點不正確的是(填字母)。
A.產(chǎn)氧和洗氣裝置組合不用一體化
B.內(nèi)部氣體流向采用高進低出方式
C.特定需求是選擇制氧方法的重要依據(jù)
D.制氧機要符合美學(xué)、工程、安全發(fā)布:2024/10/2 5:0:2組卷:72引用:3難度:0.4 -
3.學(xué)習(xí)小組開展了“設(shè)計和制作簡易供氧器”的實踐活動。
【活動一】如圖1所示,該制氧機通過A、B兩種物質(zhì)產(chǎn)生氧氣,其中A是過碳酸鈉白色固體,B是二氧化錳黑色粉末。過碳酸鈉(2Na2CO3?3H2O2)加水溶解會分解生成Na2CO3和H2O2。
?
用該制氧機制氧時,在反應(yīng)倉中加入適量水,再先后加入過碳酸鈉和二氧化錳,反應(yīng)倉內(nèi)有黑色粉末翻騰,變得渾濁,倉壁變得溫?zé)幔^濾倉底部導(dǎo)氣管口有氣泡冒出。
(1)反應(yīng)倉中H2O2生成氧氣的文字表達式是,過濾倉中的水除了有過濾雜質(zhì)提純氧氣的作用外,還可以起到的作用是(填標(biāo)號)。
A.可以通過氣泡觀察氧氣生成的速率
B.降低氧氣溫度
C.加快氧氣的生成
(2)驗證過濾倉導(dǎo)出的氣體是氧氣的方法。
(3)圖1反應(yīng)倉中“O2通道”相當(dāng)于圖2裝置中的(填“c”或“d”)導(dǎo)管。
【活動二】制作簡易的家用制氧機
(4)除需考慮反應(yīng)原理、方法選擇外,還需考慮很多方面的因素,例如:(寫一條)。同學(xué)們在充分思考交流的基礎(chǔ)上,利用家庭中常見材料,設(shè)計并制作了簡易家用制氧機(如圖),其中C瓶的作用相當(dāng)于圖2中的倉。
(5)氧氣能從圖3瓶C中逸出,是因為氧氣。
(6)根據(jù)已知信息推測,A劑的保存方法是。發(fā)布:2024/10/9 3:0:1組卷:70引用:1難度:0.5


