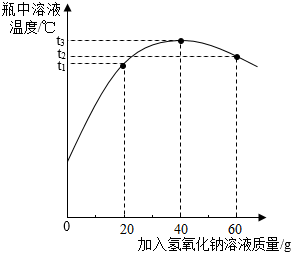
 化學(xué)小組參與“鉛蓄廢電池中硫酸回收”的研學(xué)項目,回收時需要測定電池廢液中硫酸的質(zhì)量分?jǐn)?shù)。向裝有50g廢液的錐形瓶中加入質(zhì)量分?jǐn)?shù)為20%的氫氧化鈉溶液,并充分?jǐn)嚢瑁脺囟葌鞲衅鞯入娮釉O(shè)備采集信息并繪制成如圖,請據(jù)圖回答相關(guān)問題。(雜質(zhì)可溶但不參加反應(yīng))
化學(xué)小組參與“鉛蓄廢電池中硫酸回收”的研學(xué)項目,回收時需要測定電池廢液中硫酸的質(zhì)量分?jǐn)?shù)。向裝有50g廢液的錐形瓶中加入質(zhì)量分?jǐn)?shù)為20%的氫氧化鈉溶液,并充分?jǐn)嚢瑁脺囟葌鞲衅鞯入娮釉O(shè)備采集信息并繪制成如圖,請據(jù)圖回答相關(guān)問題。(雜質(zhì)可溶但不參加反應(yīng))
(1)該反應(yīng)是 放熱放熱(選填“吸熱”或“放熱”)反應(yīng);
(2)配制上述實驗所用的氫氧化鈉溶液。用量筒量水時仰視讀數(shù),會導(dǎo)致配制的氫氧化鈉溶液質(zhì)量分?jǐn)?shù)結(jié)果 偏小偏小(選填“偏大”、“偏小”或“不變”);
(3)若雜質(zhì)忽略不計,寫出溫度為t3℃時,溶液中大量存在的分子、離子 H2O、Na+、SO2-4H2O、Na+、SO2-4(用化學(xué)符號表示)。
(4)計算廢液中硫酸的質(zhì)量分?jǐn)?shù)。
解:設(shè)廢液中硫酸的質(zhì)量為x。
2NaOH+H2SO4=Na2SO4+2H2O
80 98
40g×20% x
8098=40g×20%x8098=40g×20%x(列比例式)
求解x=9.8g
答:廢液中硫酸的質(zhì)量分?jǐn)?shù)為 9.8g50g×100%=19.6%9.8g50g×100%=19.6%(列式并計算結(jié)果)。
S
O
2
-
4
S
O
2
-
4
80
98
=
40
g
×
20
%
x
80
98
=
40
g
×
20
%
x
9
.
8
g
50
g
9
.
8
g
50
g
【考點】根據(jù)化學(xué)反應(yīng)方程式的計算;一定溶質(zhì)質(zhì)量分?jǐn)?shù)的溶液的配制;有關(guān)溶質(zhì)質(zhì)量分?jǐn)?shù)的簡單計算;物質(zhì)發(fā)生化學(xué)變化時的能量變化.
【答案】放熱;偏小;H2O、Na+、;;×100%=19.6%
S
O
2
-
4
80
98
=
40
g
×
20
%
x
9
.
8
g
50
g
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:25引用:1難度:0.5
相似題
-
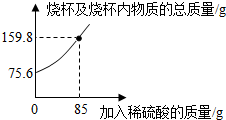 1.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為52.2g的燒杯中,然后緩慢加入一定質(zhì)量的稀硫酸,當(dāng)加稀硫酸質(zhì)量為85g時,反應(yīng)恰好完全(雜質(zhì)不反應(yīng)且產(chǎn)生的氣體全部逸出),反應(yīng)過程中的質(zhì)量關(guān)系如圖.完成下列問題:
1.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為52.2g的燒杯中,然后緩慢加入一定質(zhì)量的稀硫酸,當(dāng)加稀硫酸質(zhì)量為85g時,反應(yīng)恰好完全(雜質(zhì)不反應(yīng)且產(chǎn)生的氣體全部逸出),反應(yīng)過程中的質(zhì)量關(guān)系如圖.完成下列問題:
(1)該實驗取用的樣品質(zhì)量為g.
(2)計算樣品中鐵的質(zhì)量分?jǐn)?shù)(寫出解題過程).發(fā)布:2025/1/9 8:0:2組卷:139引用:39難度:0.1 -
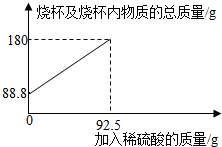 2.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分?jǐn)?shù)的稀硫酸,當(dāng)加入92.5g稀硫酸時恰好完全反應(yīng),加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系如圖。
2.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分?jǐn)?shù)的稀硫酸,當(dāng)加入92.5g稀硫酸時恰好完全反應(yīng),加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系如圖。
(1)該實驗取用的樣品質(zhì)量為g。
(2)反應(yīng)后所得溶液中的溶質(zhì)的質(zhì)量分?jǐn)?shù)。(寫出計算過程,結(jié)果保留一位小數(shù))
(3)反應(yīng)結(jié)束后,小明不慎向燒杯中多加了10g稀硫酸,若在圖中補繪此過程中稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發(fā)布:2025/1/9 8:0:2組卷:4引用:1難度:0.3 -
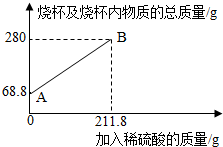 3.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分?jǐn)?shù)的稀硫酸,當(dāng)加入211.8g稀硫酸時恰好完全反應(yīng),加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系如圖。
3.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分?jǐn)?shù)的稀硫酸,當(dāng)加入211.8g稀硫酸時恰好完全反應(yīng),加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系如圖。
(1)該實驗取用的樣品質(zhì)量為g。
(2)求樣品中鐵的質(zhì)量分?jǐn)?shù);反應(yīng)后所得溶液中的溶質(zhì)的質(zhì)量分?jǐn)?shù)。(寫出計算過程,結(jié)果保留一位小數(shù))
(3)反應(yīng)結(jié)束后,小明不慎向燒杯中多加了20g稀硫酸,若在圖中補繪此過程中稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發(fā)布:2025/1/9 8:0:2組卷:8引用:1難度:0.3
相關(guān)試卷


