某溶液中只含有 Ba2+、Mg2+、Ag+三種陽離子,現用適量的 NaOH 溶液、稀鹽酸和Na2SO4溶液將這三種離子逐一沉淀分離,其流程如圖所示:
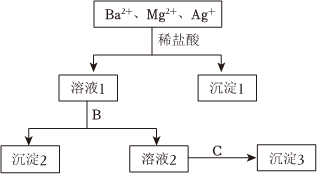
(1)沉淀1的化學式為 AgClAgCl,生成該沉淀的離子方程式為 Cl-+Ag+=AgCl↓Cl-+Ag+=AgCl↓。
(2)若試劑B為Na2SO4溶液,則沉淀2化學式為 BaSO4BaSO4。若試劑B為NaOH溶液,則沉淀2化學式為 Mg(OH)2Mg(OH)2。
(3)如果原溶液中Ba2+、Mg2+、Ag+的濃度均為0.1mol?L-1,且溶液中含有的陰離子只有NO-3,則溶液中NO-3濃度為 0.50.5mol?L-1。
NO
-
3
NO
-
3
【考點】物質分離、提純的實驗方案設計;常見離子的檢驗方法.
【答案】AgCl;Cl-+Ag+=AgCl↓;BaSO4;Mg(OH)2;0.5
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:5引用:1難度:0.6
相似題
-
1.化學家從反應C2H6(g)+Cl2(g)→C2H5Cl(l)+HCl(g)中受到啟發,提出在農藥和有機合成工業中可獲得副產品鹽酸,這一設想已成為現實.試指出從上述反應體系中得到鹽酸可采用的分離方法是( )
A.蒸餾法 B.水洗法 C.分液法 D.過濾法 發布:2024/12/30 9:30:2組卷:25引用:3難度:0.9 -
2.分離乙酸乙酯、乙醇、乙酸的混合物,可按下列步驟進行:
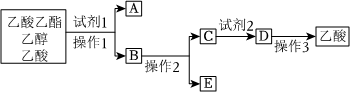
(1)試劑1最好選用。
(2)操作1是,所用的主要儀器名稱是。
(3)操作2是。
(4)試劑2最好選用。
(5)有同學認為乙酸在溫度低于16.6℃時會凝結成晶體,因此可通過降溫的方法使乙酸結晶而分離出來,操作3是結晶、過濾,這一看法是否正確?為什么?發布:2024/12/30 14:30:1組卷:13引用:5難度:0.4 -
3.苯甲酸的重結晶實驗基本操作如下:
①將粗苯甲酸1g加到100mL的燒杯中,再加入50mL蒸餾水,在石棉網上邊攪拌邊加熱,使粗苯甲酸溶解,②全溶后再加入少量蒸餾水并攪拌.③然后,使用短頸玻璃漏斗趁熱將溶液過濾到另一100mL燒杯中,將濾液靜置,使其緩慢冷卻結晶.④濾出晶體.回答下列問題:
(1)上述四步操作過程中需用到玻璃棒的步驟有
(2)步驟②的目的是;
(3)觀察濾液冷卻時的實驗現象:;
(4)重結晶后苯甲酸的狀態:.發布:2024/12/30 8:30:1組卷:45引用:4難度:0.5


