 對(duì)于N2O4(g)?2NO2(g)在溫度一定時(shí),平衡體系中NO2的體積分?jǐn)?shù)V(NO2)%隨壓強(qiáng)的變化情況如圖所示(實(shí)線(xiàn)上的任何一點(diǎn)為對(duì)應(yīng)壓強(qiáng)下的平衡點(diǎn)).
對(duì)于N2O4(g)?2NO2(g)在溫度一定時(shí),平衡體系中NO2的體積分?jǐn)?shù)V(NO2)%隨壓強(qiáng)的變化情況如圖所示(實(shí)線(xiàn)上的任何一點(diǎn)為對(duì)應(yīng)壓強(qiáng)下的平衡點(diǎn)).
(1)A、C兩點(diǎn)的反應(yīng)速率的關(guān)系為A <<C(填“>”“<”或“=”).
(2)當(dāng)反應(yīng)處于B狀態(tài)時(shí),v正==v逆(填“>”“<”或“=”),A、B、C、D、E各狀態(tài)中,v正<v逆的是 DD.
(3)由D狀態(tài)轉(zhuǎn)變?yōu)镃狀態(tài)后,混合氣體的總物質(zhì)的量會(huì) 減小減小 (填“增大”、“減小”).
(4)欲要求使E狀態(tài)從水平方向到達(dá)C狀態(tài)后,再沿平衡曲線(xiàn)達(dá)A狀態(tài),從理論上來(lái)講,可選用的條件是 BB.
A.從P1無(wú)限緩慢加壓至P2,再由P2無(wú)限緩慢降壓至P1
B.從P1突然加壓至P2,再由P2無(wú)限緩慢降壓至P1
C.從P1突然加壓至P2,再由P2突然降壓至P1.
【答案】<;=;D;減小;B
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書(shū)面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:288引用:2難度:0.5
相似題
-
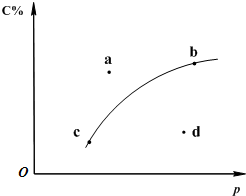 1.對(duì)于可逆反應(yīng)2A(?)+B(g)?2C(g);如圖是其它條件一定時(shí)反應(yīng)中C的百分含量與壓強(qiáng)的關(guān)系曲線(xiàn)。回答下列問(wèn)題:
1.對(duì)于可逆反應(yīng)2A(?)+B(g)?2C(g);如圖是其它條件一定時(shí)反應(yīng)中C的百分含量與壓強(qiáng)的關(guān)系曲線(xiàn)。回答下列問(wèn)題:
(1)物質(zhì)A的狀態(tài)是(填“氣體”、“液體”或“固體”);
(2)圖中a、b、c、d四點(diǎn)中表示未達(dá)到平衡狀態(tài)且v正<v逆的點(diǎn)是;
(3)在a、b、c三種條件下達(dá)平衡時(shí),v(a)、v(b)、v(c)按由大到小排序;
(4)對(duì)于2SO2(g)+O2(g)?2SO3(g);△H=-198kJ/mol。在實(shí)際生產(chǎn)過(guò)程中,原料氣中SO2為7%(體積分?jǐn)?shù))、O2為11%,常壓下進(jìn)行,控制溫度在450℃左右。
請(qǐng)問(wèn)原料氣中SO2與O2的體積比不是2:1,而要7:11(大約2:3)的原因是;如果在恒容容器中,僅把另外82%的其他氣體“抽出來(lái)”,是否會(huì)減小SO2的轉(zhuǎn)化率(填“會(huì)”或“不會(huì)”)。發(fā)布:2024/6/27 10:35:59組卷:87引用:1難度:0.3 -
2.化學(xué)中常用圖象直觀地描述化學(xué)反應(yīng)的進(jìn)程或結(jié)果。只改變一個(gè)條件,則下列對(duì)圖象的解讀正確的是( )
A. 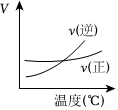
A2(g)+3B2(g)?2AB3(g)如圖說(shuō)明此反應(yīng)的正反應(yīng)是吸熱反應(yīng)B. 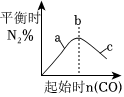
4CO(g)+2NO2(g)?N2(g)+4CO2(g)如圖說(shuō)明NO2的轉(zhuǎn)化率b>a>cC. 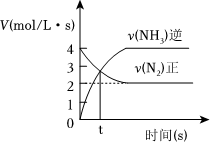
N2(g)+3H2(g)?2NH3(g)如圖說(shuō)明t秒時(shí)合成氨反應(yīng)達(dá)到平衡D. 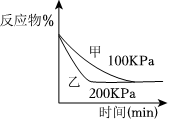
2A(g)+2B(g)?3C(g)+D(?)如圖說(shuō)明生成物D一定是氣體發(fā)布:2024/5/27 14:0:0組卷:588引用:6難度:0.4


