碳酸鈉俗稱純堿或蘇打,在生活、生產和實驗研究中均有廣泛應用。
(1)Na2CO3屬于 鹽鹽(填“酸”、“堿”、“鹽”)。
(2)若配制50g溶質質量分數為4%的Na2CO3溶液,下列操作正確的是 abab(填字母)。
a.用托盤天平稱取2gNa2CO3固體
b.選用50mL量筒量取所需體積的水
c.選用帶玻璃塞的廣口試劑瓶,將配好的溶液裝瓶并貼標簽
(3)25℃時,分別測定溶質質量分數分別為1%、2%和4%的Na2CO3溶液的pH,記錄數據如下:
| 實驗編號 | Ⅰ | Ⅱ | Ⅲ |
| 溶質質量分數 | 1% | 2% | 4% |
| 溶液pH | 11.62 | 11.76 | 11.90 |
25℃時,碳酸鈉溶液的pH隨著溶液的溶質質量分數增大而增大
25℃時,碳酸鈉溶液的pH隨著溶液的溶質質量分數增大而增大
。探究一:用Na2CO3溶液和FeSO4溶液發(fā)生復分解反應制備FeCO3
[已知溶液pH大于8.8時,Fe2+完全生成Fe(OH)2沉淀]
(4)在燒杯中制備FeCO3沉淀時,應選用的加料方式是
b
b
(填字母)。a.將FeSO4溶液與Na2CO3溶液同時加入燒杯中
b.將Na2CO3溶液緩慢加入盛有FeSO4溶液的燒杯中
c.將FeSO4溶液緩慢加入盛有Na2CO3溶液的燒杯中
d.將FeSO4溶液迅速加入盛有Na2CO3溶液的燒杯中
(5)潮濕的FeCO3固體置于空氣中易變質,生成一種紅褐色的堿,同時生成二氧化碳,該反應的化學方程式為
4FeCO3+6H2O+O2=4Fe(OH)3+4CO2
4FeCO3+6H2O+O2=4Fe(OH)3+4CO2
。探究二:興趣小組同學發(fā)現將鎂條放入Na2CO3濃溶液中,鎂條表面會產生較多氣泡,溶液中有白色沉淀生成。小組同學對此進行了探究活動。
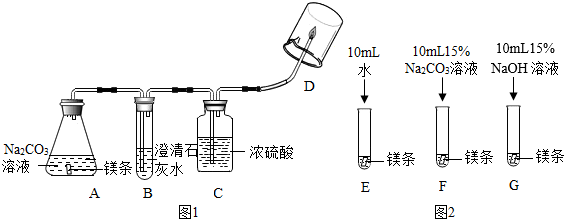
【實驗1】取適量鎂條、100mLNa2CO3溶液,按圖1所示裝置進行實驗。
觀察到A中產生較多氣泡,溶液中有白色沉淀;B中石灰水不變渾濁;D處氣體燃燒產生淡藍色火焰,杯內壁出現水珠。
(6)產生的氣體為
氫氣
氫氣
。【實驗2】按圖2所示裝置進行實驗。
【查閱資料】
①鎂能與水反應生成氣體,同時生成一種堿;
②Na2CO3溶液顯堿性,其溶液中除Na+、
CO
2
-
3
(7)觀察到E、G中緩慢產生氣泡,F中快速產生氣泡。E中反應的化學方程式為
Mg+2H2O=Mg(OH)2+H2↑
Mg+2H2O=Mg(OH)2+H2↑
。(8)比較F、G,說明溶液中促進鎂與水快速反應的微粒是
C
O
2
-
3
C
(填微粒符號)。O
2
-
3
【數據分析】小明在廚房里找到一包食用純堿,包裝袋上寫有:主要成分是碳酸鈉(質量分數>98%),雜質為氯化鈉。
(9)將21.5克該純堿樣品放入燒杯,加水完全溶解,將其放在電子秤上(如圖甲),逐漸往杯中滴加稀鹽酸,電子秤的示數與加入稀鹽酸的質量關系如圖乙所示。
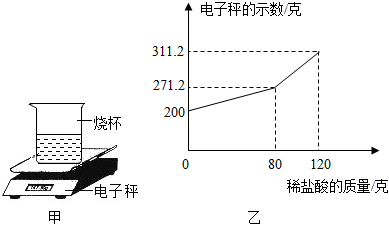
①通過計算說明,該食用純堿中碳酸鈉的質量分數是否與包裝袋信息相符
相符
相符
(計算結果精確到0.1%)。②有同學認為小明測定的食用純堿中碳酸鈉的質量分數會偏大,請分析造成碳酸鈉質量分數偏大的主要原因是
制取的二氧化碳中含有氯化氫氣體和水蒸氣,氯化氫和水蒸氣也擴散了
制取的二氧化碳中含有氯化氫氣體和水蒸氣,氯化氫和水蒸氣也擴散了
。【答案】鹽;ab;25℃時,碳酸鈉溶液的pH隨著溶液的溶質質量分數增大而增大;b;4FeCO3+6H2O+O2=4Fe(OH)3+4CO2;氫氣;Mg+2H2O=Mg(OH)2+H2↑;C;相符;制取的二氧化碳中含有氯化氫氣體和水蒸氣,氯化氫和水蒸氣也擴散了
O
2
-
3
【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網所有,未經書面同意,不得復制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:42引用:2難度:0.3
相似題
-
 1.家庭廚房就是一個充盈的化學小世界,“柴米油鹽醬醋糖”中包含著許多化學內容.
1.家庭廚房就是一個充盈的化學小世界,“柴米油鹽醬醋糖”中包含著許多化學內容.
(1)米、面的主要成分都是由三種元素組成的淀粉,淀粉屬于糖類.
(2)水瓶內的水垢主要成分是碳酸鈣,可用(填一種調味品)除去.
(3)白糖與紅糖主要成分都是蔗糖.利用活性炭的性,可將紅糖脫色成白糖.
(4)市場上銷售的香腸、鹽水鴨、榨菜、豆腐干等食品,常采用真空包裝,其目的是防止食品而變質.
(5)味精是烹制菜肴時常用的調味品,小明研究某品牌味精包裝上的部分文字說明后,想測定此味精中氯化鈉的含量.
[查閱資料]NaCl+AgNO3=AgCl↓+NaNO3,谷氨酸鈉的存在不影響NaCl性質.
[實驗過程]
①稱取該味精樣品10.0g,并溶于蒸餾水
②加入過量的硝酸銀溶液,過濾
③用蒸餾水反復洗滌沉淀多次
④將沉淀烘干、稱量,測得固體質量為5.74g
根據上述實驗步驟回答下列有關問題:
①過濾操作所需要的儀器除燒杯、鐵架臺(帶鐵圈)、玻璃棒外,還需要的玻璃儀器是.
②試通過計算確定此樣品中NaCl質量分數與其包裝上標注的含量是否相符.發(fā)布:2025/1/6 8:0:1組卷:68引用:2難度:0.5 -
2.化學興趣小組同學們在老師的指導下對市售某品牌“鈣片”的補鈣原理、成分以及功效展開了項目化學習的探究。
【查閱資料】
(1)該補鈣劑的主要成分有碳酸鈣、維生素D3、硫酸鋅、水果香料等。
(2)維生素D3、水果香料都不溶于水也不與酸反應,維生素D3主要作用是促進人體對鈣的吸收。
項目一:探究“鈣片”補鈣原理。
【分析交流】
“鈣片”中鈣以碳酸鈣形式存在,“鈣片”進入胃首先要通過人體胃酸對其進行溶解后方可被吸收。
【進行實驗】
【反思評價】服用“鈣片”時,采用實驗方案 實驗現象 實驗結論或化學方程式 取適量“鈣片”粉末于試管中,滴加足量 。化學方程式 (填“吞服”或“嚼服”)的服藥方式更有利促進胃腸吸收。
項目二:探究“鈣片”中是否含有硫酸鋅。
項目三:探究“鈣片”的功效。實驗方案 實驗現象 實驗結論 另取少量“鈣片”粉末于試管中,加足量水,充分溶解,取適量上層清液于試管中,加入幾滴 。“鈣片”中含有硫酸鋅。
【交流討論】
該補鈣劑適用于中老年人治療因缺鈣導致的患者。老師建議大家應注意平時的飲食補鈣,牛奶、魚類等食物除富含營養(yǎng)素外,是較好的補鈣食物,應該多食用。發(fā)布:2025/1/3 16:0:5組卷:30引用:1難度:0.5 -
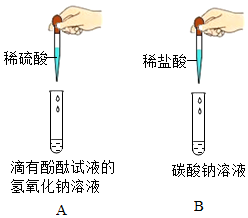 3.酸、堿、鹽種類繁多,與人類生活和生產關系密切。請回答下列問題:
3.酸、堿、鹽種類繁多,與人類生活和生產關系密切。請回答下列問題:
(1)造紙業(yè)會產生大量含NaOH的堿性廢水,需經處理至中性排放。
①寫出NaOH的俗稱:(一個即可)。
②若某造紙廠廢水中NaOH的質量分數為1.6%,現有廢硫酸9.8t(H2SO4的質量分數為10%)。可以處理的廢水質量為t。
(2)某化學興趣小組做了如圖所示的兩個實驗。完成A、B兩個實驗后,同學們將實驗后的廢液傾倒入一個廢液缸中,發(fā)現廢液呈紅色,小組同學對廢液成分展開了如下探究。(該題實驗過程中所用溶液濃度較低;氯化鈣溶液和氯化鋇溶液顯中性;實驗中如涉及硫酸鈣、氫氧化鈣等微溶物,均可看做可溶物)
【交流討論】小組同學經討論分析后一致認為廢液中一定含有的溶質有氯化鈉和(酚酞除外)。
【提出猜想】廢液中還含有的物質:
猜想一:NaOH;
猜想二:Na2CO3;
猜想三:(填化學式)。
【實驗驗證】
甲同學取少量廢液于試管中,向其中加入過量的氯化鈣溶液,通過觀察現象,得出了正確結論。若猜想二正確,甲同學觀察到的現象:有白色沉淀生成,;請寫出發(fā)生反應的化學方程式:。
【交流與反思】乙同學認為,將甲同學實驗中的氯化鈣溶液換成氯化鋇溶液,也能得出正確結論。你認為乙同學的觀點是否正確并說明你的理由:。發(fā)布:2025/1/3 8:0:1組卷:93引用:1難度:0.5


