 環己酮是重要的化工原料和化工溶劑,某研究小組對其進行了一些探究。
環己酮是重要的化工原料和化工溶劑,某研究小組對其進行了一些探究。
Ⅰ.環己酮的制備。
反應原理 Na2Cr2O7/H+55~60℃
Na2Cr2O7/H+55~60℃ ,還原產物為Cr2(SO4)3,反應過程放熱,溫度過高時環己酮易進一步被氧化,實驗裝置如圖所示。
,還原產物為Cr2(SO4)3,反應過程放熱,溫度過高時環己酮易進一步被氧化,實驗裝置如圖所示。
已知:Na2Cr2O7溶液呈橙紅色,Cr2(SO4)3溶液呈墨綠色。
(1)分液漏斗中盛放的試劑為 bb。(填字母)
a.Na2Cr2O7溶液
b.環己醇的硫酸溶液
(2)三頸燒瓶中反應體系的溫度需控制在55~60℃,其加熱方式為 向水浴中加冰水維持溫度或冰水浴或恒溫水浴向水浴中加冰水維持溫度或冰水浴或恒溫水浴。
(3)反應結束后,還需滴加甲醇,直到 溶液變為墨綠色溶液變為墨綠色(填實驗現象)為止,隨后分離提純得到環己酮。
(4)若20.0 mL環己醇(ρ=0.96g?cm-3)完全反應并提純后,得到純環己酮(ρ=0.94g?cm-3)9.6mL,則環己酮的產率為 47.9%47.9%。(計算結果保留2位有效數字)
Ⅱ.環己酮的結構與性質
(5)環己酮中三種元素的電負性由小到大的順序為 H<C<OH<C<O。(用元素符號表示)
(6)若要測定環己酮的相對分子質量,可以采用的波譜分析手段為 質譜法質譜法。
(7)已知 R“OHH+
R“OHH+ 。環己酮和乙二醇在酸性條件下反應生成分子式為C8H14O2的產物,其結構簡式為
。環己酮和乙二醇在酸性條件下反應生成分子式為C8H14O2的產物,其結構簡式為 
 。
。
N
a
2
C
r
2
O
7
/
H
+
55
~
60
℃
R
“
OH
H
+


【考點】制備實驗方案的設計.
【答案】b;向水浴中加冰水維持溫度或冰水浴或恒溫水浴;溶液變為墨綠色;47.9%;H<C<O;質譜法;

【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:14引用:2難度:0.4
相似題
-
1.硫鐵礦燒渣是硫鐵礦生產硫酸過程中產生的工業廢渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等雜質).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如圖:
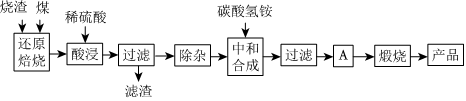
(1)在“還原焙燒”中產生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據下表數據:
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,檢驗Fe3+已經除盡的試劑是;當pH=5時,溶液中c(Al3+)=mol?L-1(已知常溫下Ksp[Al(OH)3]=2.0×10-33).
(4)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則A的操作是.
(5)a g燒渣經過上述工藝可得紅氧化鐵b g.藥典標準規定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質量分數應不低于(用含a、b的表達式表示).發布:2025/1/19 8:0:1組卷:114引用:4難度:0.5 -
2.硫鐵礦燒渣是硫鐵礦生產硫酸過程中產生的工業廢渣(主要含Fe2O3及少量SiO2、Al2O3等雜質).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如下:
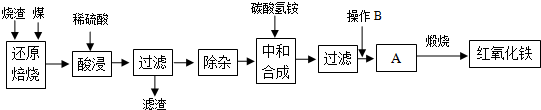
(1)在“還原焙燒”中產生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據下表數據:
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,檢驗
Fe3+已經除盡的試劑是.
(4)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則操作B是.
(5)煅燒A的反應方程式是.
(6)a g燒渣經過上述工藝可得紅氧化鐵b g.藥典標準規定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質量分數應不低于(用含a、b的表達式表示).發布:2025/1/19 8:0:1組卷:5引用:1難度:0.5 -
3.硫鐵礦燒渣是硫鐵礦生產硫酸過程中產生的工業廢渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等雜質).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如下:
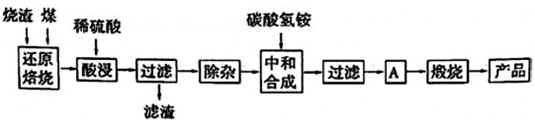
(1)在“還原焙燒”中產生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據下表數據:
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,常溫下,當pH=5時,溶液中c(Al3+)=mol?L-1(已知常溫下Ksp[Al(OH)3]═2.0×10-33).
(4)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則A的操作是.發布:2025/1/19 8:0:1組卷:12引用:1難度:0.5


