當前位置:
試題詳情
蘇州大學研究團隊對LETO材料(LiCexEu1-xTiO4)的電化學性能進行了研究,并基于微觀尺度對其進行了改進。回答下列問題:

(1)Ti的核外電子排布式為 [Ar]3d24s2[Ar]3d24s2;TiCl4分子中,Ti原子的雜化方式為 sp3sp3。
(2)第一電離能順序:IN>IO,原因是 N的價電子為2s22p3,2p軌道是半充滿,比較穩定,第一電離能較高N的價電子為2s22p3,2p軌道是半充滿,比較穩定,第一電離能較高。
(3)解釋Li的焰色現象:受熱時,Li的內層電子被激發躍遷至外層軌道,從外層軌道重新躍遷回內層軌道時,以特定波段的光能放出能量受熱時,Li的內層電子被激發躍遷至外層軌道,從外層軌道重新躍遷回內層軌道時,以特定波段的光能放出能量。
(4)某種LETO材料晶體結構示意圖如圖,晶體中O2-與Ti4+的個數比m=4:14:1。研究團隊向上述LETO材料中摻入Ce3+以改善其電化學性能,摻入Ce3+的LETO的化學式可表示為LiCexEu1-xTiOm。摻入不同數量的Ce3+時,晶格參數發生相應的變化如表所示:
| x | 0 | 0.005 | 0.010 | 0.020 |
| V/nm3 | 0.3243 | 0.3244 | 0.3249 | 0.3255 |
Ce3+的半徑大于Eu3+的半徑,導致摻入Ce3+的數目越多,晶格體積越大
Ce3+的半徑大于Eu3+的半徑,導致摻入Ce3+的數目越多,晶格體積越大
。LETO材料依靠填充在TiOm多面體層間的Li+的遷移導電,隨著x值的增大,推測材料的導電性能力將 增強
增強
(填“增強”“減弱”或“不變”)。(5)Ni2+與Li+半徑大小接近,但在晶格中很難遷移,當LETO材料中混有Ni2+時,Ni2+會部分取代
Li+
Li+
(填“Li+”“Ti4+”“Eu3+”或“O2-”)的位置,這可能會導致 ABC
ABC
(填選項標號)。A.Li+在材料中遷移困難
B.充放電循環穩定性欠佳
C.電容量損失
【答案】[Ar]3d24s2;sp3;N的價電子為2s22p3,2p軌道是半充滿,比較穩定,第一電離能較高;受熱時,Li的內層電子被激發躍遷至外層軌道,從外層軌道重新躍遷回內層軌道時,以特定波段的光能放出能量;4:1;Ce3+的半徑大于Eu3+的半徑,導致摻入Ce3+的數目越多,晶格體積越大;增強;Li+;ABC
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:10引用:1難度:0.7
相似題
-
1.回答下列問題
(1)肼(N2H4)分子可視為NH3分子中的一個氫原子被-NH2取代形成的另一種氮的氫化物。
①NH3分子的空間結構是;N2H4分子中氮原子軌道的雜化類型是。
②肼可用作火箭燃料,燃燒時發生的反應是N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)ΔH=-1038.7kJ?mol-1,若該反應中有4molN-H斷裂,則形成的π鍵有mol。
③肼能與硫酸反應生成N2H6SO4,N2H6SO4與硫酸銨化合物類型相同,則N2H6SO4晶體不存在(填標號)。
a.離子鍵
b.共價鍵
c.范德華力
(2)第ⅥA族元素氧、硫、硒(Se)的化合物在研究和生產中有許多重要用途。請回答下列問題:
①H2Se的還原性比H2S(填“強”或“弱”)。氣態SeO3分子的空間結構為,SO2的VSEPR模型為,空間結構為。
②H2O內的O-H、水分子間的范德華力和氫鍵,從強到弱依次為,H+可與H2O形成H3O+,H3O+中O采用雜化,H3O+中H-O-H鍵角比H2O中的(填“大”或“小”)發布:2025/1/5 8:0:1組卷:21引用:1難度:0.6 -
2.下列化學用語或圖示正確的是( )
A.NH3和 的VSEPR模型和空間結構均一致NH+4B. 的VSEPR模型:SO2-3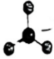
C.丙酮( 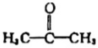 )分子中C原子的雜化類型均是sp2
)分子中C原子的雜化類型均是sp2D.HCl分子中σ鍵的形成: 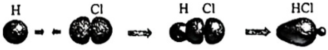 發布:2025/1/5 8:0:1組卷:24引用:2難度:0.5
發布:2025/1/5 8:0:1組卷:24引用:2難度:0.5 -
3.當地時間2020年1月30日晚,世界衛生組織(WHO)宣布,將新型冠狀病毒疫情列為國際關注的突發公共衛生事件,防疫專家表示,75%的醫用酒精、含氯消毒劑(如84消毒液等)可以有效殺滅病毒,佩戴口罩能有效減少感染新冠的危險。下列有關說法正確的是( )
A.制作口罩的原料之一丙烯分子中存在sp2-sp2和sp2-sp3σ鍵 B.乙醇可以和水以任意比互溶的原因只是因為兩者均為極性分子,相似相溶 C.次氯酸的電子式: 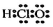
D.乙醇分子中官能團為羥基,在水中形成分子內氫鍵 發布:2025/1/6 6:0:5組卷:6引用:1難度:0.7


