化學電源在生產生活中有著廣泛的應用,請回答下列問題:
(1)理論上講,任何自發的氧化還原反應都可以設計成原電池。請利用反應“Cu+2Ag+═2Ag+Cu2+”設計一個化學電池,回答下列問題:該電池的負極材料是 CuCu,發生 氧化氧化(填“氧化”或“還原”)反應,電解質溶液是 AgNO3溶液AgNO3溶液。
(2)為了探究化學反應中的能量變化,某同學設計了如圖1所示兩個實驗(圖Ⅰ、圖Ⅱ中除連接的銅棒不同外,其他均相同),有關實驗現象,下列說法正確的是 ADAD。
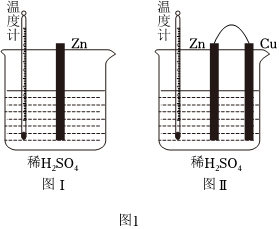
A.圖Ⅰ中溫度計的示數高于圖Ⅱ的示數
B.圖Ⅰ和圖Ⅱ中溫度計的示數相等,且均高于室溫
C.圖Ⅰ和圖Ⅱ的氣泡均產生于鋅棒表面
D.圖Ⅱ中產生氣體的速度比Ⅰ快
(3)有甲、乙兩位同學均想利用原電池反應檢測金屬的活動性順序,兩人均用鎂片和鋁片作電極,但甲同學將電極放入6mol?L-1的H2SO4溶液中,乙同學將電極放入6mol?L-1的NaOH溶液中,如圖2所示。
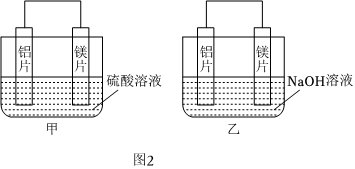
①裝置甲中放電時氫離子向 鋁片鋁片(填“鎂片”或“鋁片”)移動。寫出甲中正極的電極反應式:2H++2e-=H2↑2H++2e-=H2↑。
②裝置乙中鋁片為 負負極,寫出該電極的電極反應式 Al-3e-+4OH-=AlO-2+2H2OAl-3e-+4OH-=AlO-2+2H2O。
③如果甲與乙同學均認為“構成原電池的電極材料都是金屬時,則構成負極材料的金屬應比構成正極材料的金屬活潑”,由此他們會得出不同的結論。依據該實驗得出的下列結論中,正確的有 ADAD。
A.利用原電池反應判斷金屬活動性順序時應注意選擇合適的介質
B.鎂的金屬性不一定比鋁的金屬性強
C.該實驗說明金屬活動性順序表已過時,沒有實用價值了
D.該實驗說明化學研究對象復雜、反應受條件影響較大,因此具體問題應具體分析
A
l
O
-
2
A
l
O
-
2
【考點】原電池與電解池的綜合.
【答案】Cu;氧化;AgNO3溶液;AD;鋁片;2H++2e-=H2↑;負;Al-3e-+4OH-=+2H2O;AD
A
l
O
-
2
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:128引用:2難度:0.6
相似題
-
1.某原電池結構如圖所示,下列有關該原電池的說法正確的是( )
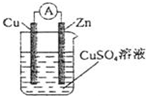
A.銅棒為負極 B.鋅棒發生還原反應 C.電子從銅棒經外電路流向鋅棒 D.鋅棒質量減輕 發布:2025/1/6 6:0:5組卷:417引用:11難度:0.9 -
2.關于如圖所示的原電池,下列說法正確的是( )
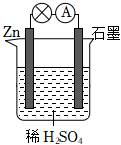
A.石墨電極上發生氧化反應 B.電子由鋅片通過導線流向石墨棒 C.該裝置將電能轉化為化學能 D.將稀硫酸換成乙醇,燈泡亮度不變 發布:2025/1/6 6:0:5組卷:83引用:5難度:0.8 -
3.一種新型短路膜電化學電池消除CO2裝置如圖所示。下列說法錯誤的是( )
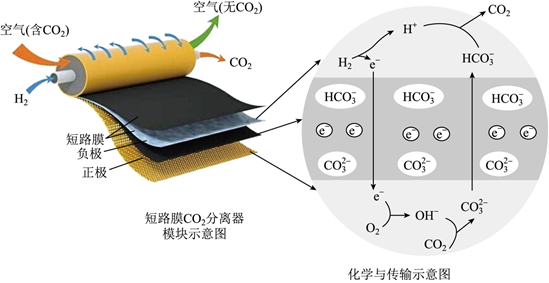
A.負極反應為:H2+2OH--2e-=2H2O B.正極反應消耗標準狀況下22.4LO2,理論上需要轉移4mol電子 C.短路膜和常見的離子交換膜不同,它既能傳遞離子,還可以傳遞電子 D.該裝置可用于空氣中CO2的捕獲,緩解溫室效應 發布:2024/12/30 19:30:2組卷:51引用:5難度:0.5


