水合肼(N2H4?H2O)及其衍生物在許多工業(yè)中被廣泛的使用,沸點118℃,有強還原性,在空氣中可吸收二氧化碳而產(chǎn)生煙霧。實驗室利用NaClO氧化尿素制備水合肼分為以下兩步:
I、制備次氯酸鈉
II、與尿素[CO(NH2)2]在堿性條件下反應制備水合肼,實驗裝置如圖所示(部分裝置省略):

(1)裝置B的作用是儲存多余的Cl2,可用的試劑是 飽和氯化鈉溶液飽和氯化鈉溶液。
(2)裝置C中制備NaClO的反應過程中溫度升高易產(chǎn)生副產(chǎn)物NaClO3,實驗中可采取的措施是 進行冰水浴進行冰水浴(寫一條即可)。
(3)將裝置C中制備的溶液轉(zhuǎn)移到裝置D的 三頸燒瓶三頸燒瓶(填儀器名稱)中,并緩緩滴入,原因是 防止生成的水合肼被NaClO氧化防止生成的水合肼被NaClO氧化,裝置D中生成水合肼的化學方程式為 CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4?H2O+NaClCO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4?H2O+NaCl(在此反應中有蘇打生成)。
(4)有同學認為該實驗收集裝置有缺陷,請你寫出改進措施 收集裝置與外界連通的導管應連接一個裝有堿石灰的干燥管收集裝置與外界連通的導管應連接一個裝有堿石灰的干燥管。
(5)常溫時,水合肼在堿性條件下可以還原銀氨溶液來回收金屬銀,并產(chǎn)生無污染氣體N2,寫出該反應的離子方程式:4[Ag(NH3)2]++N2H4?H2O+4OH-=4Ag↓+N2↑+8NH3↑+5H2O4[Ag(NH3)2]++N2H4?H2O+4OH-=4Ag↓+N2↑+8NH3↑+5H2O。
(6)稱取3.0g水合肼樣品,加水配制成250mL溶液,從中取出25.00mL溶液于錐形瓶中,滴入幾滴淀粉溶液,用0.300mol/L的I溶液進行滴定,滴定終點的現(xiàn)象 當?shù)稳胱詈蟀氲蜪2溶液,溶液顏色變成藍色,且半分鐘內(nèi)不褪色時即達到滴定終點當?shù)稳胱詈蟀氲蜪2溶液,溶液顏色變成藍色,且半分鐘內(nèi)不褪色時即達到滴定終點,測得消耗I2溶液的體積為27.50mL,則樣品中水合肼(N2H4?H2O)的質(zhì)量百分數(shù)為 68.8%68.8%(保留3位有效數(shù)字)。 (已知:N2H4?H2O+2I2═N2↑+4HI+H2O)
(7)滴定時,下列能導致水合肼的含量測定結(jié)果偏低的是 abcabc(填字母)
a.實驗過程中,部分HI被空氣氧化
b.滴定前,盛標準液的滴定管內(nèi)無氣泡,滴定后有氣泡
c.讀數(shù)時,滴定前仰視,滴定后俯視
d.盛標準液的滴定管水洗后,直接裝標準液
【答案】飽和氯化鈉溶液;進行冰水浴;三頸燒瓶;防止生成的水合肼被NaClO氧化;CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4?H2O+NaCl;收集裝置與外界連通的導管應連接一個裝有堿石灰的干燥管;4[Ag(NH3)2]++N2H4?H2O+4OH-=4Ag↓+N2↑+8NH3↑+5H2O;當?shù)稳胱詈蟀氲蜪2溶液,溶液顏色變成藍色,且半分鐘內(nèi)不褪色時即達到滴定終點;68.8%;abc
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:39引用:3難度:0.4
相似題
-
1.硫鐵礦燒渣是硫鐵礦生產(chǎn)硫酸過程中產(chǎn)生的工業(yè)廢渣(主要含F(xiàn)e2O3及少量SiO2、Al2O3等雜質(zhì)).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如下:
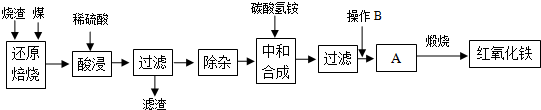
(1)在“還原焙燒”中產(chǎn)生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據(jù)下表數(shù)據(jù):
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,檢驗
Fe3+已經(jīng)除盡的試劑是.
(4)“中和合成”的目的是將溶液中Fe2+轉(zhuǎn)變?yōu)樘妓醽嗚F沉淀,則操作B是.
(5)煅燒A的反應方程式是.
(6)a g燒渣經(jīng)過上述工藝可得紅氧化鐵b g.藥典標準規(guī)定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質(zhì)量分數(shù)應不低于(用含a、b的表達式表示).發(fā)布:2025/1/19 8:0:1組卷:5引用:1難度:0.5 -
2.硫鐵礦燒渣是硫鐵礦生產(chǎn)硫酸過程中產(chǎn)生的工業(yè)廢渣(主要含F(xiàn)e2O3及少量SiO2、Al2O3、CaO、MgO等雜質(zhì)).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如圖:
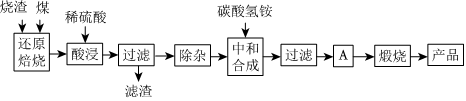
(1)在“還原焙燒”中產(chǎn)生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據(jù)下表數(shù)據(jù):
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,檢驗Fe3+已經(jīng)除盡的試劑是;當pH=5時,溶液中c(Al3+)=mol?L-1(已知常溫下Ksp[Al(OH)3]=2.0×10-33).
(4)“中和合成”的目的是將溶液中Fe2+轉(zhuǎn)變?yōu)樘妓醽嗚F沉淀,則A的操作是.
(5)a g燒渣經(jīng)過上述工藝可得紅氧化鐵b g.藥典標準規(guī)定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質(zhì)量分數(shù)應不低于(用含a、b的表達式表示).發(fā)布:2025/1/19 8:0:1組卷:114引用:4難度:0.5 -
3.硫鐵礦燒渣是硫鐵礦生產(chǎn)硫酸過程中產(chǎn)生的工業(yè)廢渣(主要含F(xiàn)e2O3及少量SiO2、Al2O3、CaO、MgO等雜質(zhì)).用該燒渣制取藥用輔料--紅氧化鐵的工藝流程如下:
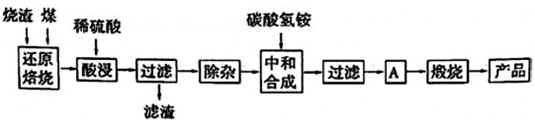
(1)在“還原焙燒”中產(chǎn)生的有毒氣體可能有.
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示).
(3)根據(jù)下表數(shù)據(jù):
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,常溫下,當pH=5時,溶液中c(Al3+)=mol?L-1(已知常溫下Ksp[Al(OH)3]═2.0×10-33).
(4)“中和合成”的目的是將溶液中Fe2+轉(zhuǎn)變?yōu)樘妓醽嗚F沉淀,則A的操作是.發(fā)布:2025/1/19 8:0:1組卷:12引用:1難度:0.5
相關(guān)試卷


