當前位置:
試題詳情
氮的氧化物(NOx)是大氣污染物之一,工業(yè)上在一定溫度和催化劑條件下用NH3將NOx還原生成N2。某同學在實驗室中對NH3與NOx反應(yīng)進行了探究。回答下列問題:
(1)氨氣的制備。
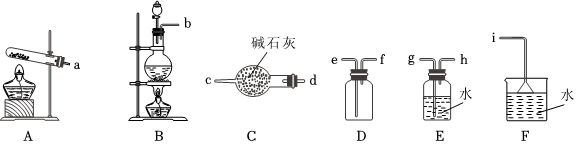
①氨氣的發(fā)生裝置可以選擇圖中的 AA,反應(yīng)的化學方程式為 2NH4Cl+Ca(OH)2 △ 2NH3↑+CaCl2+2H2O2NH4Cl+Ca(OH)2 △ 2NH3↑+CaCl2+2H2O。
②欲收集一瓶干燥的氨氣,選擇圖中的裝置,其連接順序為:發(fā)生裝置→d→c→f→e→id→c→f→e→i(按氣流方向,用小寫字母表示)。
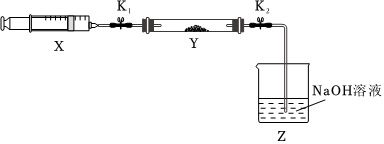
(2)氨氣與二氧化氮的反應(yīng):將上述收集到的NH3充入注射器X中,硬質(zhì)玻璃管Y中加入少量催化劑,充入NO2(用夾子K1、K2夾好)。在一定溫度下按圖示裝置進行實驗。
△
△
| 操作步驟 | 實驗現(xiàn)象 | 解釋原因 |
| 打開K1,推動注射器活塞,使X中的氣體緩慢通入Y管中 | ①Y管中 紅棕色氣體慢慢變淺 紅棕色氣體慢慢變淺 |
②反應(yīng)的化學方程式 8NH3+6NO2 催化劑 8NH3+6NO2 催化劑 |
| 將注射器活塞退回原處并固定,待裝置恢復到室溫 | Y管中有少量水珠 | 生成的氣態(tài)水凝聚 |
| 打開K2 | ③ 溶液倒吸入Y管 溶液倒吸入Y管 |
④反應(yīng)后氣體分子數(shù)減少,Y管中壓強小于外壓 |
4NO2+O2+2Na2CO3=4NaNO3+2CO2
4NO2+O2+2Na2CO3=4NaNO3+2CO2
,空氣的作用是 提供氧化劑
提供氧化劑
。【答案】A;2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O;d→c→f→e→i;紅棕色氣體慢慢變淺;8NH3+6NO2 7N2+12H2O;溶液倒吸入Y管;4NO2+O2+2Na2CO3=4NaNO3+2CO2;提供氧化劑
△
催化劑
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:22引用:1難度:0.5
相似題
-
1.甲、乙、丙三位同學分別用圖1所示實驗裝置制取氨氣.請你根據(jù)實驗探究的過程,回答下列有關(guān)問題.

(1)三位同學制取氨氣的化學方程式是.
(2)三位同學用上述裝置制取氨氣時,其中有一位同學沒有收集到氨氣(實驗操作都正確),你認為沒有收集到氨氣的同學是(填圖1中“甲”、“乙”或“丙”).
(3)為確定試管內(nèi)是否已收集滿氨氣,應(yīng)將置于收集氣體的試管口處,若觀察到,則說明氨氣已收集滿.
(4)三位同學都認為他們的實驗裝置還可用于加熱碳酸氫銨固體來制取純凈的氨氣,你判斷能夠達到實驗?zāi)康耐瑢W是(填圖1中“甲”、“乙”或“丙”).
(5)氨氣是一種重要的化工產(chǎn)品,氨氣經(jīng)一系列反應(yīng)可制得硝酸,其中關(guān)鍵步驟之一是將二氧化氮溶于水生成硝酸.為使二氧化氮盡可能全部被水吸收,且殘留的氣體盡可能少,某同學設(shè)計了如圖2所示的實驗裝置,進行了如下實驗探究過程.請回答有關(guān)問題.實驗過程 實驗現(xiàn)象 步驟一 將收集滿NO2的集氣瓶倒立在水槽中. 集氣瓶中液面上升;集氣瓶中氣體由紅棕色變成無色;最終剩余氣體約占集氣瓶體積的 .步驟二 將分液漏斗中的水逐滴滴入燒瓶,使少量O2進入盛有NO2的集氣瓶后,停止滴水. 集氣瓶中氣體顏色的變化情況是 ;集氣瓶中液面繼續(xù)上升.步驟三 多次重復步驟二操作,并依次減少O2通入量,直至O2通入后,氣體不再變成 色.現(xiàn)象與步驟二相同,最后集氣瓶內(nèi)幾乎充滿液體,只含極少量氣體. 計算 用上述實驗方法,將標準狀況下448mLNO2全部溶于水,得到500mL溶液,則溶液中HNO3的物質(zhì)的量濃度為 .發(fā)布:2024/12/30 5:0:1組卷:64引用:3難度:0.3 -
 2.某化學研究小組的同學在實驗室中利用如圖裝置制取并收集少量干燥NH3。下列敘述正確的是( )
2.某化學研究小組的同學在實驗室中利用如圖裝置制取并收集少量干燥NH3。下列敘述正確的是( )A.試管a中的固體是NH4Cl和NaOH的混合物 B.裝置b中的試劑是堿石灰 C.用塞子代替棉花,收集到的NH3純度更高 D.用蘸有濃硫酸的玻璃棒靠近c試管口能檢驗NH3是否收集滿 發(fā)布:2024/12/30 7:30:1組卷:129引用:2難度:0.8 -
3.實驗室制取少量干燥的氨氣涉及下列裝置,其中正確的是( )
A. 
氨氣發(fā)生裝置B. 
氨氣吸收裝置C. 
氨氣發(fā)生裝置D. 
氨氣收集、檢驗裝置發(fā)布:2024/12/30 5:30:2組卷:36引用:6難度:0.9


