自然界中存在大量的金屬元素,其中鈉、鎂、鋁、鐵、銅等在工農(nóng)業(yè)生產(chǎn)中有著廣泛的應(yīng)用。回答下列問題: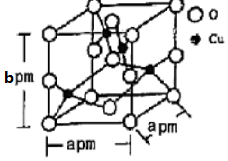
(1)CuSO4和Cu(NO3)2中陽離子核外電子排布式為1s22s22p63s23p63d91s22s22p63s23p63d9,N、O、S元素的原子對(duì)鍵合電子吸引力最大的是OO。
(2)在硫酸銅溶液中加入過量KCN能生成配離子[Cu(CN)4]2-,1mol CN-中含有的π鍵的數(shù)目為2NA或2×6.02×10232NA或2×6.02×1023。與CN-互為等電子體的離子或分子有C22-、CO、N2;C22-、CO、N2;(寫出一種即可)。
(3)[Cu(NH3)4]2+中,提供孤對(duì)電子的是NH3NH3。Cu(NH3)2Cl2有兩種同分異構(gòu)體,其中一種可溶于水,則此種化合物是極性極性(填“極性”或“非極性”)分子,由此推知[Cu(NH)4]2+的空間構(gòu)型是平面正方形平面正方形。(填“平面正方形”或“正四面體”)
(4)NH3中N原子的雜化方式是sp3sp3,硫元素對(duì)應(yīng)的含氧酸酸性是H2SO4強(qiáng)于H2SO3,其原因?yàn)?!--BA-->H2SO4與H2SO3分別可表示為(HO)2SO2和(HO)2SO,前者非羥基氧(2個(gè))多于后者的非羥基氧(1個(gè))的數(shù)目,使H2SO4中的S-O-H中的O的電子更偏向于S,越容易電離出H+,酸性更強(qiáng)H2SO4與H2SO3分別可表示為(HO)2SO2和(HO)2SO,前者非羥基氧(2個(gè))多于后者的非羥基氧(1個(gè))的數(shù)目,使H2SO4中的S-O-H中的O的電子更偏向于S,越容易電離出H+,酸性更強(qiáng)。
(5)銅的一種氧化物晶體結(jié)構(gòu)如圖所示,該氧化物的化學(xué)式是CuOCuO。若該晶體結(jié)構(gòu)為長方體,其參數(shù)如圖,阿伏加德羅常數(shù)為NA,則該氧化物的密度為320NA?a2b×10-30320NA?a2b×10-30g/cm3。
320
N
A
?
a
2
b
×
10
-
30
320
N
A
?
a
2
b
×
10
-
30
【答案】1s22s22p63s23p63d9;O;2NA或2×6.02×1023;C22-、CO、N2;;NH3;極性;平面正方形;sp3;H2SO4與H2SO3分別可表示為(HO)2SO2和(HO)2SO,前者非羥基氧(2個(gè))多于后者的非羥基氧(1個(gè))的數(shù)目,使H2SO4中的S-O-H中的O的電子更偏向于S,越容易電離出H+,酸性更強(qiáng);CuO;
320
N
A
?
a
2
b
×
10
-
30
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:30引用:2難度:0.5
相似題
-
 1.著名化學(xué)家徐光憲在稀土化學(xué)等領(lǐng)域取得了卓越成就,被譽(yù)為“稀土界的袁隆平”。稀土元素包括鈧、釔和鑭系元素。
1.著名化學(xué)家徐光憲在稀土化學(xué)等領(lǐng)域取得了卓越成就,被譽(yù)為“稀土界的袁隆平”。稀土元素包括鈧、釔和鑭系元素。
請(qǐng)回答下列問題:
(1)寫出基態(tài)二價(jià)鈧離子(Sc2+)的核外電子排布式,其中
電子占據(jù)的軌道數(shù)為。
(2)在用重量法測定鑭系元素和使鑭系元素分離時(shí),總是使之先轉(zhuǎn)換成草酸鹽,然后
經(jīng)過灼燒而得其氧化物,如2LnCl3+3H2C2O4+nH2O=Ln2(C2O4)3?nH2O+6HCl。
①H2C2O4中碳原子的雜化軌道類型為;1 mol H2C2O4分子中含σ鍵和π鍵的數(shù)目之比為。
②H2O的VSEPR模型為;寫出與H2O互為等電子體的一種陰離子的化學(xué)式。
③HCl和H2O可以形成相對(duì)穩(wěn)定的水合氫離子鹽晶體,如HCl?2H2O,HCl?2H2O中含有H5O2+,結(jié)構(gòu)為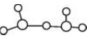 ,在該離子中,存在的作用力有
,在該離子中,存在的作用力有
a.配位鍵b。極性鍵c。非極性鍵d。離子鍵e。金屬鍵f。氫鍵g。范德華力 h.π鍵i。σ鍵
(3)表列出了核電荷數(shù)為21~25的元素的最高正化合價(jià):
對(duì)比上述五種元素原子的核外電子排布與元素的最高正化合價(jià),你發(fā)現(xiàn)的規(guī)律是元素名稱 鈧 鈦 釩 鉻 錳 元素符號(hào) Sc Ti V Cr Mn 核電荷數(shù) 21 22 23 24 25 最高正價(jià) +3 +4 +5 +6 +7
(4)PrO2(二氧化鐠)的晶胞結(jié)構(gòu)與CaF2相似,晶胞中Pr(鐠)原子位于面心和頂點(diǎn)。假設(shè)相距最近的Pr原子與O原子之間的距離為a pm,則該晶體的密度為g?cm-3(用NA表示阿伏加德羅常數(shù)的值,不必計(jì)算出結(jié)果)。發(fā)布:2025/1/5 8:0:1組卷:29引用:1難度:0.6 -
2.新型鈣鈦礦太陽能電池具備更加清潔、便于應(yīng)用、制造成本低和效率高等顯著優(yōu)點(diǎn)。 一種鈣鈦礦太陽能電池材料的晶胞如圖1所示。請(qǐng)按要求回答下列有關(guān)問題
(1)構(gòu)成CH3NH3+的三種元素中電負(fù)性最小的是; 寫出碳原子的電子排布式為。
(2)Pb與C同主族,比C的周期序數(shù)大4,寫出Pb原子最外層電子的軌道表示式(即電子排布圖)。
(3)有關(guān)NH3的結(jié)構(gòu)與性質(zhì)探究
①NH3分子中所含化學(xué)鍵是(從“極性鍵”、“非極性鍵”、“配位鍵”、“離子鍵”、“σ鍵”或“π鍵”中選填符合的名稱);N原子的雜化形式為。
②NH3分子的VSEPR模型名稱為,分子的空間結(jié)構(gòu)(即立體構(gòu)型) 為。
③如圖2所示,探究NH3的性質(zhì)時(shí),打開止水夾,擠壓膠頭滴管,可以觀察到燒瓶中迅速產(chǎn)生紅色噴泉。請(qǐng)用必要的分子結(jié)構(gòu)與性質(zhì)的知識(shí)和化學(xué)用語解釋產(chǎn)生該現(xiàn)象的原因:、。
(4)該鈣鈦礦太陽能電池材料的化學(xué)式為;該晶胞中,與I-緊鄰的I-個(gè)數(shù)為; 測定其晶體結(jié)構(gòu)特征最可靠的方法是實(shí)驗(yàn)。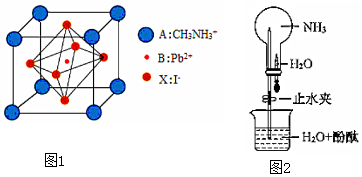 發(fā)布:2025/1/5 8:0:1組卷:85引用:1難度:0.5
發(fā)布:2025/1/5 8:0:1組卷:85引用:1難度:0.5 -
3.下列各組表述中,正確的是( )
A.基態(tài)核外電子的排布為1s22s22p63s23p4的原子3p能級(jí)有一個(gè)空軌道 B.第四周期中,未成對(duì)電子數(shù)最多的原子為Mn C.Fe2+的基態(tài)核外電子排布為1s22s22p63s23p63d6 D.2P能級(jí)有2個(gè)未成對(duì)電子的基態(tài)原子的價(jià)電子排布一定為2s22p2 發(fā)布:2025/1/6 6:0:5組卷:50引用:3難度:0.7


