研究物質的溶解對于生產、生活有著重要意義。
下表是碳酸鈉的部分溶解度數據。
| 溫度/℃ | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| 溶解度/g | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 | 45.1 | 44.7 |
易溶
易溶
物質(填“易溶”“可溶”“微溶”或“難溶”)。(2)由表中數據可知,碳酸鈉的溶解度隨溫度升高
先增大后減小(合理即可)
先增大后減小(合理即可)
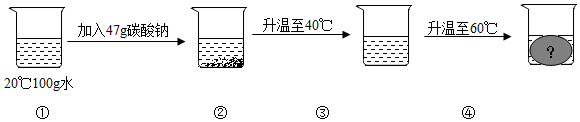
。(3)小東同學進行了如圖所示的實驗,若使燒杯③中的溶液達到飽和,至少需再加入
1.8
1.8
g碳酸鈉;升溫至60℃時,燒杯④中會出現的現象是 有晶體析出
有晶體析出
。
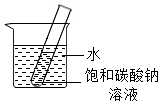
(4)20℃時,將裝有飽和碳酸鈉溶液(底部有碳酸鈉粉末)的小試管放入盛水的燒杯中(如圖)。向燒杯中加入某物質后,試管底部的粉末減少,則加入的物質可能是
A
A
(填字母序號),該物質形成的溶液中存在的微粒有 Na+、OH-、H2O
Na+、OH-、H2O
。
A.氫氧化鈉
B.碳酸鈣
C.硝酸銨
D.氯化鈉
【答案】易溶;先增大后減小(合理即可);1.8;有晶體析出;A;Na+、OH-、H2O
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:761引用:10難度:0.5
相似題
-
1.溶液在日常生活、工農業生產和科學研究中具有廣泛用途。氫氧化鈣、硝酸鉀、氯化鈉的溶解度如下表所示。
回答問題:溫度/℃ 0 20 40 60 80 溶解度/g 氫氧化鈣 0.18 0.16 0.14 0.11 0.09 硝酸鉀 13.3 31.6 63.9 110 169 氯化鈉 35.7 36.0 36.6 37.3 38.4
(1)氫氧化鈣的溶解度隨溫度的升高而(選填“增大”或“減小”)。
(2)將接近飽和的硝酸鉀溶液變為飽和溶液,可采取的方法有、。(任寫兩種)
(3)農業上常用質量分數為16%的氯化鈉溶液選種。20℃時,將136g飽和氯化鈉溶液稀釋成質量分數為16%的氯化鈉溶液,需加水的質量為。
(4)下列有關說法正確的是(填序號)。
A.40℃時,向氫氧化鈣飽和溶液中加入少量硝酸鉀,溶液質量變大
B.60℃時,將100g硝酸鉀飽和溶液恒溫蒸發10g水,析出11g硝酸鉀
C.某物質的不飽和溶液,其溶質的質量分數可能比該物質的飽和溶液大
D.將80℃時上述三種物質的飽和溶液各mg分別降溫至20℃,所得溶液中,氯化鈉溶液的質量最大發布:2024/8/7 8:0:9組卷:35引用:1難度:0.6 -
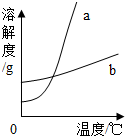 2.KNO3和KCl在不同溫度時的溶解度如下表所示.請回答下列問題:
2.KNO3和KCl在不同溫度時的溶解度如下表所示.請回答下列問題:
(1)依據上表數據,繪制KNO3和KCl的溶解度曲線,如圖中能表示KNO3溶解度曲線的是溫度/℃ 0 10 20 30 40 50 60 70 溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 KCl 27.6 31.0 34.0 37.0 40.0 42.6 45.5 48.3 .(填“a”或“b”)
(2)由表中數據分析可知,KNO3和KCl在某一溫度時具有相同的溶解度x,則x的取值范圍是:.
(3)10℃時,131g 飽和KCl溶液,蒸發10g水后,再降溫到10℃,可析出KCl晶體的質量為.
(4)欲將60℃時不飽和硝酸鉀溶液變成飽和溶液,下列說法正確的是.
A.溶液中溶劑的質量可能減少 B.溶液中溶質的質量可能增加
C.溶液中溶質的質量分數一定增大 D.溶液中溶質的質量分數可能不變.發布:2024/9/13 15:0:8組卷:107引用:3難度:0.5


