為了測定空氣中氧氣的含量,甲乙兩組同學分別進行了如下實驗。
【實驗探究一】:甲組同學對教材中“測定空氣里氧氣含量”的實驗(如圖1)進行了大膽改進,設計如圖2(選用容積為30mL的硬質試管作反應容器)實驗方案進行,收到了良好的效果。請你對比分析下面圖1、圖2實驗,回答下列有關問題:

(1)圖1實驗中發生反應的符號表達式為 P+O2點燃P2O5P+O2點燃P2O5。
(2)圖2實驗的操作步驟如下(固定試管和注射器的儀器已省略):
①點燃酒精燈,不斷推動注射器活塞
②撤去酒精燈
③將少量紅磷平裝入試管中,將20mL的注射器活塞置于10mL刻度處,并按圖2中所示的連接方式固定好。
④待冷卻后,讀取注射器活塞的數據。
你認為正確的實驗操作順序是 ③①②④③①②④(填序號)。
(3)圖2實驗中,注射器活塞將從10mL刻度處慢慢前移到約為 44mL刻度處才停止。
(4)與圖1實驗對比,圖8實驗的優點是 實驗結果更準確或更環保實驗結果更準確或更環保。(寫出一點即可)
【實驗探究二】:乙組同學設計出如圖3所示的實驗裝置,實驗時在銅絲末端的燃燒匙中放足量白磷。圖4為用氣體壓力傳感器測得的廣口瓶中氣壓變化情況,通過初始壓強(P1)與反應結束后的壓強(P2),可以計算出氧氣的體積分數:O2%=(P1-P2)/P1×100%。回答有關問題:

(5)用酒精燈加熱銅絲一端,可觀察到銅絲表面產生的現象是 由紅色變黑色由紅色變黑色,寫出該反應的符號表達式 Cu+O2△CuOCu+O2△CuO。
(6)圖4中B→C→D段氣壓變化的原因是 B→C段,白磷燃燒放熱導致氣壓增大幅度大于氧氣消耗導致氣壓減小幅度;C→D段,氧氣消耗,溫度降低B→C段,白磷燃燒放熱導致氣壓增大幅度大于氧氣消耗導致氣壓減小幅度;C→D段,氧氣消耗,溫度降低。
(7)導致DE段氣壓變化的實驗操作是 打開彈簧夾打開彈簧夾。
(8)該實驗測得空氣中氧氣的含量是 20.8%20.8%(精確到0.1%)。
點燃
點燃
△
△
【考點】測定空氣里氧氣含量的探究.
【答案】P+O2P2O5;③①②④;4;實驗結果更準確或更環保;由紅色變黑色;Cu+O2CuO;B→C段,白磷燃燒放熱導致氣壓增大幅度大于氧氣消耗導致氣壓減小幅度;C→D段,氧氣消耗,溫度降低;打開彈簧夾;20.8%
點燃
△
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/9/5 3:0:9組卷:16引用:1難度:0.5
相似題
-
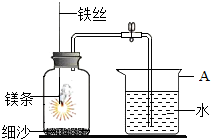 1.某校研究性學習小組用如圖所示裝置進行鎂條在空氣中燃燒的實驗。待鎂條完全燃燒并冷卻后打開彈簧夾,進入集氣瓶中水的體積約占集氣瓶容積的70%。
1.某校研究性學習小組用如圖所示裝置進行鎂條在空氣中燃燒的實驗。待鎂條完全燃燒并冷卻后打開彈簧夾,進入集氣瓶中水的體積約占集氣瓶容積的70%。
(1)圖中A儀器的名稱是。鎂條燃燒并冷卻后打開彈簧夾,水能進入到集氣瓶中的原因是。
(2)如果鎂條只和空氣中的氧氣反應,則進入集氣瓶中水的體積最多不超過其容積的%.現進入集氣瓶中水的體積約為其容積的70%,根據空氣的組成可推出減少的氣體中有氮氣。
【發現問題】氮氣是如何減少的?
【做出猜想】。
【查閱資料】鎂條在氮氣中能燃燒,產物為氮化鎂(Mg3N2)固體。氮化化鎂中氮的化合價是。鎂條還可以在二氧化碳氣體中燃燒生成碳和氧化鎂,反應的化學方程式為2Mg+CO2C+2MgO,該反應所的基本反應類型是點燃。
(3)通過以上探究,你對燃燒的有關知識有了哪些新的認識?(寫出一條即可)
(4)24g鎂在二氧化碳中燃燒可生成多少克氧化鎂?發布:2024/11/18 8:0:1組卷:13引用:1難度:0.5 -
2.如圖1是某化學興趣小組利用氣壓傳感器測定紅磷燃燒時集氣瓶內氣壓變化的實驗裝置。圖2是集氣瓶內氣壓隨時間的變化情況。下列說法不正確的是( )
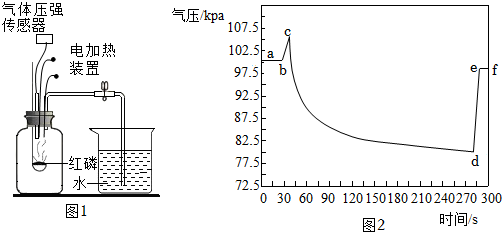
A.bc段氣壓增大的主要原因是紅磷燃燒放熱 B.cd段氣壓減小的主要原因是集氣瓶內氧氣不斷被消耗 C.紅磷熄滅后,若立即打開止水夾會導致測得的結果小于 15D.若用木炭代替紅磷,集氣瓶內氣壓變化趨勢與圖2基本一致 發布:2024/12/25 11:30:2組卷:1085引用:3難度:0.7 -
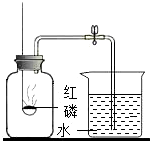 3.測定空氣里氧氣的含量,甲、乙、丙三個同學用如圖所示的裝置分別進行了實驗探究。
3.測定空氣里氧氣的含量,甲、乙、丙三個同學用如圖所示的裝置分別進行了實驗探究。
(1)實驗時,取下橡膠塞,點燃紅磷后迅速伸入集氣瓶中并旋緊橡膠塞,這時看到的現象是,該反應的文字表達式為。
(2)甲同學:用足量的木炭代替紅磷做測定空氣中氧氣含量的實驗,結果實驗失敗了,請你幫助他分析失敗的原因:。
(3)乙同學:想用鎂條來代替紅磷做實驗,老師告訴他這種方法不是較好的方法,因為鎂條在空氣中燃燒非常劇烈,鎂既可以和氧氣反應,也可以和氮氣反應生成氮化鎂。請寫出鎂和氮氣反應生成氮化鎂的文字表達式:。
(4)丙同學:打算用鐵絲替代紅磷,實驗能否成功?請說明理由。。
(5)燃燒后,集氣瓶內剩余的氣體主要是氮氣,請結合本實驗推測氮氣的物理性質是。發布:2024/11/7 8:0:2組卷:19引用:1難度:0.5


