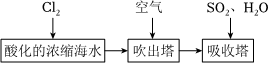
工業以濃縮海水為原料提取溴的部分過程如圖:
某課外小組在實驗室模擬上述過程設計以下裝置進行實驗(所有橡膠制品均已被保護,夾持裝置已略去):
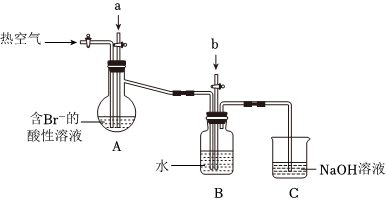
(1)實驗開始時,A裝置中不通熱空氣,先通入a氣體的目的是(用離子方程式表示) Cl2+2Br-═2Cl-+Br2Cl2+2Br-═2Cl-+Br2。
(2)反應過程中,B裝置中Br2與SO2反應的化學方程式:SO2+Br2+2H2O═H2SO4+2HBrSO2+Br2+2H2O═H2SO4+2HBr。
(3)C裝置的作用是 吸收未反應完的Cl2、Br2、SO2等有毒氣體,防止污染空氣吸收未反應完的Cl2、Br2、SO2等有毒氣體,防止污染空氣。
(4)該小組同學向反應后B裝置的溶液中通入氯氣,充分反應得到混合液。
①一位同學根據溴的沸點是59℃,提出采用 蒸餾蒸餾方法從該混合液中分離出溴單質。
②另一位同學向該混合液中加入四氯化碳,充分振蕩、靜置后放出下層液體,這種方法是 萃取分液萃取分液。
(5)某同學提出證明反應后B裝置的溶液中含有溴離子的實驗方案是:取出少量溶液,先加入過量新制氯水,再加入KI淀粉溶液,觀察溶液是否變藍色。
該方案是否合理并簡述理由:不合理,氯水可能過量不合理,氯水可能過量。
【考點】從海水中提取溴.
【答案】Cl2+2Br-═2Cl-+Br2;SO2+Br2+2H2O═H2SO4+2HBr;吸收未反應完的Cl2、Br2、SO2等有毒氣體,防止污染空氣;蒸餾;萃取分液;不合理,氯水可能過量
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:46引用:2難度:0.5
相似題
-
1.海洋中有豐富的食品、礦產、能源、藥物和水產資源,下圖為海水利用的部分過程。下列有關說法不正確的是( )
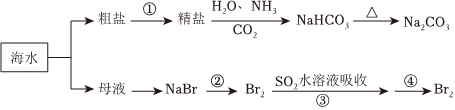
A.制取NaHCO3的反應是利用其溶解度小于NaCl B.侯氏制堿應先通NH3再通CO2 C.在第②、③、④步驟中,溴元素均被氧化 D.③④的目的是進行溴的富集 發布:2024/12/30 3:30:1組卷:129引用:9難度:0.6 -
2.海水是化學元素的寶庫,從海水中可以提取或生產多種化工原料,如食鹽、氯氣、單質溴、鎂、純堿等,它們在工農業生產中有著廣泛的用途.根據學過的知識回答下列問題:
(1)某化學興趣小組計劃用氯氣和氫氧化鈉制取簡易消毒液.
①其反應原理為:(用離子方程式表示).
②配制250mL 4.0mol?L-1NaOH溶液,需要用到的玻璃儀器,除燒杯、玻璃棒外,還必須用到的是.
(2)工業制得粗硅后,再與氯氣等物質發生反應,最終得到純硅.請寫出工業制取粗硅的化學方程式:
(3)金屬鎂被譽為“國防金屬”,若鎂起火,不能用CO2來滅火,其原因可用化學方程式表示為
(4)①若Na2CO3固體中混有少量NaHCO3雜質,除去雜質的方法是,
②若NaHCO3溶液中混有少量Na2CO3雜質,除去雜質的方法是.發布:2024/10/27 17:0:2組卷:11引用:1難度:0.5 -
3.海水資源開發利用的部分過程如圖所示:
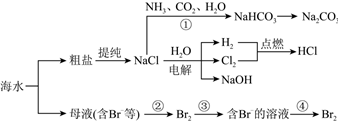
下列說法正確的是( )A.粗鹽(含Mg2+、Ca2+、 等)提純所加試劑順序為NaOH→Na2CO3→BaCl2→過濾→HClSO2-4B.過程①為了提高產率一般先通CO2再通NH3 C.用澄清石灰水可以鑒別NaHCO3和Na2CO3溶液 D.過程②③④可以達到富集溴的目的 發布:2024/11/3 6:0:1組卷:50引用:3難度:0.7


