某班同學分成A、B兩組,并分別設計如下實驗探究能較長時間觀察到白色Fe(OH)2沉淀的制取方法。回答下列問題:A組實驗:用NaOH溶液和FeSO4溶液直接反應。(如圖1)
(1)FeSO4由鐵粉還原Fe2(SO4)3制得寫出反應離子方程式:Fe+2Fe3+=3Fe2+Fe+2Fe3+=3Fe2+。
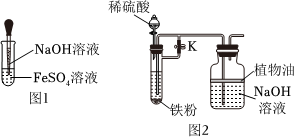
(2)該方法能觀察到白色的Fe(OH)2沉淀,但沉淀顏色快速發生變化,其顏色變化為 先生成白色沉淀,迅速轉化為灰綠色,一段時間后變為紅褐色先生成白色沉淀,迅速轉化為灰綠色,一段時間后變為紅褐色。請分析沉淀顏色變化的原因:4Fe(OH)2+O2+2H2O=4Fe(OH)34Fe(OH)2+O2+2H2O=4Fe(OH)3(用化學方程式表示)B組實驗:選用稀硫酸、鐵粉、NaOH溶液進行實驗,裝置如圖2。
(3)實驗時,先 打開打開(填“打開”或“關閉”)止水夾K,然后打開 分液漏斗分液漏斗的玻璃塞和活塞,使稀硫酸與鐵粉反應,一段時間后,關閉關閉(填“打開”或“關閉”)止水夾K,制得白色Fe(OH)2沉淀,且沉淀能一段時間不變色,原因是 稀硫酸與鐵粉作用產生的H2排出了裝置中的空氣稀硫酸與鐵粉作用產生的H2排出了裝置中的空氣。
【考點】制取氫氧化鐵、氫氧化亞鐵.
【答案】Fe+2Fe3+=3Fe2+;先生成白色沉淀,迅速轉化為灰綠色,一段時間后變為紅褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3;打開;分液漏斗;關閉;稀硫酸與鐵粉作用產生的H2排出了裝置中的空氣
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:42引用:4難度:0.7
相似題
-
 1.如圖所示裝置可用來制取和觀察Fe(OH)2在空氣中被氧化時的顏色變化.實驗時必須使用鐵屑和6mol?L-1的硫酸,其他試劑任選.填寫下列空白:
1.如圖所示裝置可用來制取和觀察Fe(OH)2在空氣中被氧化時的顏色變化.實驗時必須使用鐵屑和6mol?L-1的硫酸,其他試劑任選.填寫下列空白:
(1)B中盛有一定量的NaOH溶液,A中應預先加入的試劑是,A中反應的離子方程式是.
(2)實驗開始時應先將活塞E(填“打開”“關閉”或“無關系”),C中收集到氣體的主要成分是.
(3)關閉活塞E及分液漏斗上的活塞加入適量硫酸,硫酸與鐵屑接觸后產生氣體.待收集到足量氣體后關閉活塞E,現象是.
(4)拔去裝置B中的橡皮塞,使空氣進入,寫出有關反應的化學方程式:.發布:2024/8/8 8:0:9組卷:71引用:5難度:0.1 -
2.下列物質中,不能直接與水反應制取的是( )
A.H2SO4 B.NaOH C.H2CO3 D.Fe(OH)3 發布:2024/7/14 8:0:9組卷:1引用:1難度:0.7 -
 3.實驗室可用如圖裝置制備Fe(OH)2。下列說法不正確的是( )
3.實驗室可用如圖裝置制備Fe(OH)2。下列說法不正確的是( )A.配制NaOH溶液和FeSO4溶液的蒸餾水要提前煮沸 B.實驗前可在FeSO4溶液上面加一層煤油 C.得到的Fe(OH)2為紅褐色固體 D.實驗結束后的膠頭滴管,要先用鹽酸浸泡,再用水洗 發布:2024/8/8 8:0:9組卷:137引用:2難度:0.5


