B、D、C、A、E 五種元素的原子序數順序依次增大,其中只有E為金屬元素,D、C 元素在元素周期表中位置相鄰,在一定條件下,B 的單質可以分別和A、C、D 的單質化合生成甲、乙、丙化合物,C 的單質和D 的單質化合可得丁,戊、己、庚均為化合物。已知乙、丙每個分子中均含有10 個電子,圖為相互轉化關系:

請回答下列問題:
(1)寫出E 的原子結構示意圖
 。
。
(2)寫出C、D 氫化物的穩定性由強到弱的順序H2O>NH3H2O>NH3(用化學式表示)。
(3)A、B、D 三種元素形成的化合物中其中一種可用作化肥,寫該化合物的電子式
 。
。
(4)寫出C與丙反應的化學反應方程式4NH3+5O2催化劑△4NO+6H2O4NH3+5O2催化劑△4NO+6H2O。
(5)寫出工業上從海水中制取A 的離子反應方程式2Cl-+2H2O 電解 Cl2↑+H2↑+2OH-2Cl-+2H2O 電解 Cl2↑+H2↑+2OH-。
(6)工業上通過如下轉化可制得含A 元素的鉀鹽KAO3 晶體:NaA溶液80℃,通電ⅠNaAO3室溫,KAⅡKAO3晶體
①完成Ⅰ中反應的總化學方程式:NaCl+3 H2O 通電 NaClO3+3 H2↑NaCl+3 H2O 通電 NaClO3+3 H2↑。
□NaA+□H2O 通電 □NaAO3+□3 H2↑3 H2↑
②Ⅱ中反應過程能析出KClO3晶體而無其他晶體析出的原因是室溫下,氯酸鉀在水中的溶解度明顯小于其他晶體室溫下,氯酸鉀在水中的溶解度明顯小于其他晶體。




催化劑
△
催化劑
△
電解
電解
80
℃
,
通電
Ⅰ
室溫
,
KA
Ⅱ
通電
通電
通電
【考點】無機物的推斷.
【答案】 ;H2O>NH3;
;H2O>NH3; ;4NH3+5O24NO+6H2O;2Cl-+2H2O Cl2↑+H2↑+2OH-;NaCl+3 H2O NaClO3+3 H2↑;3 H2↑;室溫下,氯酸鉀在水中的溶解度明顯小于其他晶體
;4NH3+5O24NO+6H2O;2Cl-+2H2O Cl2↑+H2↑+2OH-;NaCl+3 H2O NaClO3+3 H2↑;3 H2↑;室溫下,氯酸鉀在水中的溶解度明顯小于其他晶體
 ;H2O>NH3;
;H2O>NH3; ;4NH3+5O2
;4NH3+5O2催化劑
△
電解
通電
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:15引用:2難度:0.3
相似題
-
1.如圖是部分短周期元素的單質及其化合物(或其溶液)的轉化關系,已知B、C、D、E是非金屬單質,且在常溫常壓下都是氣體;化合物G的焰色反應為黃色,化合物I和J通常狀況下呈氣態;
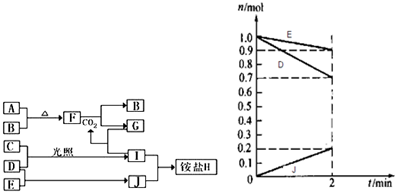
請完成下列填空:
(1)H的化學式;其晶體中所含化學鍵類型為;檢驗H 中陽離子的方法是.
(2)A與B 在加熱條件下反應的主要現象是;F和H2O反應的化學方程式為;寫出G溶液中加入過量的I溶液反應的離子方程式.
(3)某溫度時,在2L容器中,D、E、J三種物質的物質的量隨時間變化的曲線如圖所示.由圖中數據分析:該反應的化學方程式為.反應開始至2min,用J表示的平均反應速率為.發布:2024/12/30 15:0:1組卷:6引用:3難度:0.3 -
2.已知某物質X 能發生如下轉化:X
YO2①ZO2②A。下列有關上述轉化關系中物質及其反應的敘述錯誤的是( )H2O③A.若X為NH3,則A為硝酸 B.若X為H2S,則A為亞硫酸或者硫酸 C.反應①和②一定為氧化還原反應,反應③有可能為非氧化還原反應 D.若X為非金屬單質或非金屬氫化物,則A 一定能與金屬銅反應生成Y 發布:2025/1/6 6:0:5組卷:28引用:2難度:0.5 -
3.通常情況下,微粒A和B為分子,C和E為陽離子,D為陰離子,它們都含有10個電子;B溶于A后所得的物質可電離出C和D;A、B、E三種微粒反應后可得C和一種白色沉淀.請回答.
(1)用化學符號表示下列微粒:C:,D:.
(2)寫出A、B、E三種微粒反應的離子方程式:.發布:2024/12/30 17:0:2組卷:48引用:19難度:0.5


